题目内容
8.下列叙述正确的是( )| A. | 蛋白质溶液中加入Na2SO4溶液可使其变性 | |
| B. | 氨基酸具有两性,既能与酸反应又能与碱反应 | |
| C. | 蔗糖既能发生水解反应,又能发生银镜反应 | |
| D. | 纤维素在人体内不能水解生成葡萄糖,因此对人体健康无益 |
分析 A.Na2SO4可使蛋白质发生盐析;
B.氨基酸含羧基和氨基分析;
C.蔗糖为二糖,不含-CHO;
D.人体内不含水解纤维素的酶.
解答 解:A.Na2SO4可使蛋白质发生盐析,加入重金属盐发生变性,故A错误;
B.氨基酸含羧基和氨基,既能与酸反应又能与碱反应属于两性化合物,故B正确;
C.蔗糖为二糖,不含-CHO,是非还原性糖,则蔗糖能发生水解反应,不能发生银镜反应,故C错误;
D.人体内不含水解纤维素的酶,所以不能消化纤维素,但人类膳食中的纤维素主要含于蔬菜和粗加工的谷类中,虽然不能被消化吸收,但有促进肠道蠕动,利于粪便排出等功能,故D错误.
故选B.
点评 本题考查了氨基酸、蛋白质、糖类的结构性质的分析应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
7.反应mA(g)+nB(g)≒pC(g)在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表所示:
分析表中数据,回答:
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡不(填“向左”“向右”或“不”)移动,理由是平衡没有移动,即m+n=p.
(2)当压强从5×105 Pa增加到1×106 Pa 时,该反应的化学平衡向左移动,判断的依据是当压强增大2倍时,c(A)却增加了2.2倍,说明平衡向生成A的方向移动,可能的原因是增大压强时,B转化为液态或固态.
| 压强/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/(mol•L-1) | 0.08 | 0.20 | 0.44 |
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡不(填“向左”“向右”或“不”)移动,理由是平衡没有移动,即m+n=p.
(2)当压强从5×105 Pa增加到1×106 Pa 时,该反应的化学平衡向左移动,判断的依据是当压强增大2倍时,c(A)却增加了2.2倍,说明平衡向生成A的方向移动,可能的原因是增大压强时,B转化为液态或固态.
19.下列图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确的是( )


| A. | 石墨转变为金刚石是吸热反应 | |
| B. | 白磷比红磷稳定 | |
| C. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| D. | CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
3.两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2.E的单质与水蒸气反应,生成一种黑色固体Y.请回答下列问题:
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
①乙组得到的黑色粉末是FeO.
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色固体粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
20.下列叙述Ⅰ和Ⅱ均正确并且互为因果关系的是( )
| 选项 | 叙 述Ⅰ | 叙 述Ⅱ |
| A | NH3溶于水显碱性 | 用氨气作“喷泉实验” |
| B | 高锰酸钾具有强氧化性 | 高锰酸钾须与活性金属粉末分开储存 |
| C | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| D | 碘在酒精中溶解度大于在水中溶解度 | 用酒精萃取碘水中的碘 |
| A. | A | B. | B | C. | C | D. | D |
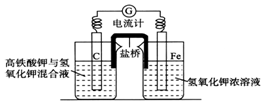 高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中.如图甲是高铁电池的实验装置:已知放电后,两极得到铁的相同价态的化合物.
高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中.如图甲是高铁电池的实验装置:已知放电后,两极得到铁的相同价态的化合物. 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题: