题目内容
同周期的X、Y、Z三元素,其最高价氧化物水化物的酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则下列判断正确的是( )
| A、原子半径 X>Y>Z |
| B、非金属性X>Y>Z |
| C、阴离子的还原性 X->Y2->Z3- |
| D、气态氢化物的稳定性 HX<H2Y<ZH3 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:同周期元素从左到右,非金属性逐渐增强,则对应的最高价氧化物水化物的酸性逐渐增强,酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则非金属性:Z<Y<X,原子序数Z<Y<X,以此解答该题.
解答:
解:同周期元素从左到右,非金属性逐渐增强,则对应的最高价氧化物水化物的酸性逐渐增强,酸性由弱到强的顺序是:H3ZO4<H2YO4<HXO4,则非金属性:Z<Y<X,原子序数Z<Y<X,
A.同周期元素原子序数Z<Y<X,同周期元素从左到右,元素的原子半径逐渐减小,则原子半径X<Y<Z,故A错误;
B.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,则非金属性Z<Y<X,故B正确;
C.非金属性Z<Y<X,元素的非金属性越强,对应单质的氧化性越强,则阴离子的还原性越弱,故C错误;
D.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,对应氢化物的稳定性逐渐增强,故D错误.
故选B.
A.同周期元素原子序数Z<Y<X,同周期元素从左到右,元素的原子半径逐渐减小,则原子半径X<Y<Z,故A错误;
B.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,则非金属性Z<Y<X,故B正确;
C.非金属性Z<Y<X,元素的非金属性越强,对应单质的氧化性越强,则阴离子的还原性越弱,故C错误;
D.同周期元素原子序数Z<Y<X,同周期元素从左到右,非金属性逐渐增强,对应氢化物的稳定性逐渐增强,故D错误.
故选B.
点评:本题考查元素周期律的递变规律,为高频考点,侧重于学生分析的能力的考查,题目难度中等,本题的解答关键是根据酸性判断非金属性和原子序数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某温度和压强下,将4g由三种炔烃组成的混合气体与足量的氢气反应,充分加成后,生成4.4g三种对应的烷烃,则所得烷烃中一定有( )
| A、异丁烷 | B、乙烷 | C、丙烷 | D、丁烷 |
下列各溶液中,Na+浓度最大的是( )
| A、4L0.5 mol?L-1NaCl溶液 |
| B、1L0.3 mol?L-1的Na2SO4溶液 |
| C、0.8L0.4 mol?L-1NaOH溶液 |
| D、2L0.15 mol?L-1Na3PO4溶液 |
下列卤代烃,既能发生水解反应,又能发生消去反应的是( )
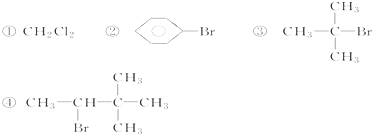

| A、①② | B、③④ | C、②④ | D、①③ |
已知断裂1mol C-H键,要吸收热量414.4kJ;断裂1mol C-C键,要吸收热量347.4kJ;生成1mol C═C键,会放出热量615.3kJ;生成1mol H-H键,会放出热量435.3kJ,某有机物分解的反应可表示为: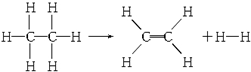
若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )

若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )
| A、该反应放出251.2 kJ的热量 |
| B、该反应吸收251.2 kJ的热量 |
| C、该反应放出125.6 kJ的热量 |
| D、该反应吸收125.6 kJ的热量 |
固体熔化时,必须破坏非极性共价键的是( )
| A、冰 | B、晶体硅 | C、溴 | D、二氧化硅 |
下列各指定微粒的数目比不是1:1的是( )
| A、Na2O2晶体中阴离子和阳离子 | ||
| B、NaHSO4晶体中阳离子和阴离子 | ||
C、
| ||
| D、氯化钠中的质子总数和电子总数 |
在密闭容器中于一定条件下进行下列反应:2SO2+O2?2SO3当到达平衡时通入18O2,再次平衡时,18O存在于( )
| A、SO2、O2 |
| B、SO2、SO3 |
| C、O2、SO3 |
| D、SO2、O2、SO3 |