题目内容
【题目】某校化学兴趣小组为制备消毒液(主要成分是NaClO),设计了下列装置,并查阅到下边资料:在加热情况下氯气和碱溶液能发生反应:3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O。
5Cl-+ClO3-+3H2O。

请回答下列问题:
(1)连接好装置,装药品之前,必须进行的一项操作步骤是________________。
(2)圆底烧瓶内发生反应的化学方程式为____________________________;大试管内发生反应的离子方程式为_______________________________________。
(3)饱和食盐水的作用是_____________;冰水的作用是___________________。
(4)在制取C12时,实验室中若无MnO2,可用KMnO4粉末代替,发生下列反应:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的发生装置是_____(填序号)。

【答案】 检查装置的气密性 MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O Cl2+2OH-=Cl-+ClO-+H2O 除去Cl2中的HCl气体 防止溶液温度升高而发生副反应 AD
MnCl2+Cl2↑+2H2O Cl2+2OH-=Cl-+ClO-+H2O 除去Cl2中的HCl气体 防止溶液温度升高而发生副反应 AD
【解析】
(1)连接好装置,装药品之前,必须进行的操作是检查装置的气密性;
(2)二氧化锰与浓盐酸加热产生氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;大试管内发生反应是氯气与氢氧化钠溶液的反应,反应方程式为Cl2+2OH-=Cl-+ClO-+H2O;
MnCl2+Cl2↑+2H2O;大试管内发生反应是氯气与氢氧化钠溶液的反应,反应方程式为Cl2+2OH-=Cl-+ClO-+H2O;
(3)在制取氯气的反应中浓盐酸易挥发,用饱和食盐水除去氯气中的氯化氢气体;温度较高时,能够发生副反应3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O,因此冰水的作用是防止溶液温度升高而发生副反应;
5Cl-+ClO3-+3H2O,因此冰水的作用是防止溶液温度升高而发生副反应;
(4)根据反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O可知,不需要加热,所以图2中AD装置都可以。

【题目】碳酸钙可用作食品添加剂。以磷石膏(主要成分为CaSO4·2H2O)为原料制备碳酸钙的一种工艺流程如下:

(1)已知磷石膏“水洗”前后的部分杂质质量分数变化如下表:
SiO2 | P2O5 | Al2O3 | F- | Fe2O3 | |
水洗前/% | 9.21 | 3.08 | 0.55 | 0.68 | 0.19 |
水洗后/% | 8.96 | 1.37 | 0.46 | 0.29 | 0.27 |
则“水洗“除去的主要杂质是___________。
(2)气体A的化学式为_______。
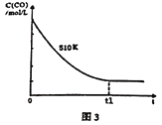
(3)“碳化”时发生反应的化学方程式为____________。其他条件一定时,“碳化”反应中CaSO4的转化率随温度的变化如右图所示,温度高于45℃,CaSO4的转化率下降的原因是________。

(4)工业上电解(NH4)2SO4溶液可制取过二硫酸铵[(NH4)2S2O8],其中S2O82-的结构如下。电解时阳极的电极反应式为__________,过二硫酸铵可用于游泳池中水的消毒,其原因是_________。