题目内容
天然气的主要成分是甲烷(CH4),甲烷燃烧时的能量变化如右图所示。
⑴ 写出甲烷完全燃烧生成CO2和气态水的热化
学方程式:
_________________________________________
![]() ⑵ 已知H2O (l) H2O(g) ΔH = +44kJ/mol,则甲烷完全燃烧生成CO2和18g液态水,放出的热量是_________________
⑵ 已知H2O (l) H2O(g) ΔH = +44kJ/mol,则甲烷完全燃烧生成CO2和18g液态水,放出的热量是_________________
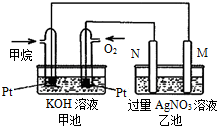
⑶ 美国科学家设计出以甲烷为燃料的新型燃料电池,其成本大大低于以氢气为燃料的传统燃料电池。甲烷燃料电池的电解质溶液为KOH,请写出该电池工作时的总反应方程式:
_________________________________________
右图中,_____(填“a”或“b”)极为正极
⑷ 若用⑶中的甲烷燃料电池为电源,以石墨作为电极,电解熔融NaCl,当生成92g金属Na时,甲烷燃料电池消耗标准状况下的甲烷的体积是__________


⑴ CH4(g)+ 2O2(g)=== CO2(g)+ 2H2O(g)ΔH = -802kJ/mol 3’ ⑵ 445kJ 3’
⑶ CH4 + 2O2 + 2KOH === K2CO3 + 3H2O 2’ b 1’ ⑷ 11.2L 3’

 走进文言文系列答案
走进文言文系列答案合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料。从天然气获得合成气过程中可能发生的反应有:
① CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
② CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
2CO(g)+2H2(g) ΔH2=+247.3 kJ/mol
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3
CO2(g)+H2(g) ΔH3
请回答下列问题:
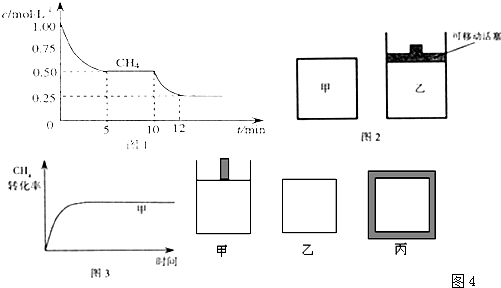
⑴ 在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。反应进行的前5 min内, v(H2)= ▲ ;10 min时,改变的外界条件可能是 ▲ 。
|

⑵ 如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间变化的图像如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。

⑶ 反应③中ΔH3= ▲ 。800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应③中正、逆反应速率的关系式是 ▲ (填代号)。
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断



 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.
天然气的主要成分甲烷燃烧生成二氧化碳和液态水的热化学方程式如下,请回答下列问题:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ/mol.