题目内容
 (2013?朝阳区二模)铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:
(2013?朝阳区二模)铅蓄电池是最常见的二次电池,其构造示意图如下.发生反应的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)
| 放电 |
| 充电 |
分析:A.放电时,正极上得电子发生还原反应;
B.充电时,该装置是电解池,电源正极应该与B连接;
C.电解精炼铜时,粗铜应该接电源正极;
D.根据转移电子守恒解答.
B.充电时,该装置是电解池,电源正极应该与B连接;
C.电解精炼铜时,粗铜应该接电源正极;
D.根据转移电子守恒解答.
解答:解:A.放电时,正极上得电子发生还原反应,电极反应式为:PbO2(s)+4H+(aq)+SO42-(aq)+2e-═PbSO4(s)+2H2O(l),故A正确;
B.充电时,要使该装置恢复原状,电解池阳极上应该失电子发生氧化反应,所以应将外接直流电源的正极与铅蓄电池的接线柱B相接,故B错误;
C.电解精炼铜时,粗铜应该接电源正极,该装置作原电池时,二氧化铅作正极,所以应将粗铜与接线柱B相连接,故C正确;
D.铅蓄电池做电源电解Na2SO4溶液时,当有2mol O2产生时,转移电子8mol,当转移8mol电子时需要消耗8mol H2SO4,故D正确;
故选B.
B.充电时,要使该装置恢复原状,电解池阳极上应该失电子发生氧化反应,所以应将外接直流电源的正极与铅蓄电池的接线柱B相接,故B错误;
C.电解精炼铜时,粗铜应该接电源正极,该装置作原电池时,二氧化铅作正极,所以应将粗铜与接线柱B相连接,故C正确;
D.铅蓄电池做电源电解Na2SO4溶液时,当有2mol O2产生时,转移电子8mol,当转移8mol电子时需要消耗8mol H2SO4,故D正确;
故选B.
点评:本题考查原电池和电解池原理,注意铅蓄电池充放电时各电极上发生的反应,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

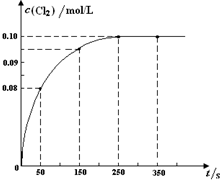 (2013?朝阳区二模)温度为T时,向2L恒容密闭容器中充入1mol PCl5,发生PCl5(g)?PCl3(g)+Cl2(g)反应.反应过程中c(Cl2) 随时间变化的曲线如图所示,下列说法不正确的是( )
(2013?朝阳区二模)温度为T时,向2L恒容密闭容器中充入1mol PCl5,发生PCl5(g)?PCl3(g)+Cl2(g)反应.反应过程中c(Cl2) 随时间变化的曲线如图所示,下列说法不正确的是( )