��Ŀ����
��09�γǵ����ε��У�һЩ�ϻ��õĽ�����ijЩ�ض��Ľ��ʻ����У����Ϊ����״̬���������ڽ��������ϸ�����һ������Ĥ�����ڲ�ͬŨ�ȵ��������ܽ���ۻ������ͼ��ʾ����̽���������⣺
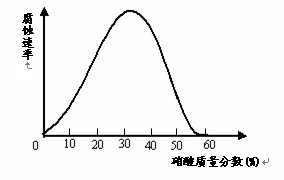
��1������һö��������������ʹ������γɶۻ��㣬Ӧ�������Ũ�ȴ��� ��������һ��ʱ�䣻֤����������γ�һ�����ܵĶۻ���ļ�ʵ���ǣ� �������������� ��
��2�������й�˵������ȷ���� ��ѡ����ţ���
![]()
A��ͭ���������Ũ���ᣬ����Ϊͭ��Ũ�����з����ۻ�
B��ͭƬ����Ƭ�õ������Ӻ�������Ũ�����У�����һ��������ͭ�缫�ص�����������
C������������Һ�еĸ�ʴ����������Ũ��һ��������
D���������Ũ�����ȥ���������ڵ�ˮ��
��3������Һ����NaNO3��NaNO2��NaOH��ɵģ��ڼ��������£�ͨ��������Ӧʹ����������һ�����ܵ�Fe3O4��3Fe+NaNO2+5NaOH![]() 3Na2FeO2+H2O+NH3�����������٣�
3Na2FeO2+H2O+NH3�����������٣�
8Fe+3NaNO3+5NaOH+2H2O![]() 4Na2Fe2O4+3NH3�������ڣ�
4Na2Fe2O4+3NH3�������ڣ�
�Լ������������������������벹���������Ӧ�ķ���ʽ����ƽ�� ��
��4��Ϊ��ʹ�������γɽϺ������Ĥ����ҵ�ϳ��õ��������Һ�ķ�������������������������д����ʱ�����ĵ缫��Ӧ�� ��
��1��57%(��ֵ����55%����)��
ȡ������ݺ����������CuSO4��ϡ���ᣩ��Һ�У���������û�к�ɫ�����ʣ����ݣ�����
��2��ABC
��3��Na2FeO2+Na2Fe2O4+2H2O=Fe3O4��+4NaOH
��4��3H2O+2Al��6e��=Al2O3+6H+

 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д���09�γǵ����ε��У��Ȼ����dz�����ˮ����������ˮFeCl3���۵�Ϊ555K���е�Ϊ588K����ҵ���Ʊ���ˮFeCl3��һ�ֹ������£�
��1��ȡ0.5mL���Ȼ�����Һ����50mL��ˮ�У������Ƭ�̵ú��ɫ��Һ�壬�ù��̿������ӷ���ʽ��ʾΪ�� ��
��2����֪��ˮ���Ȼ�����ˮ�е��ܽ�����£�
�¶�/��. | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
�ܽ��(g/100gH20) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
��FeCl3��Һ�л��FeCl3?6H2O�ķ����ǣ� ��
��3�����������¶ȳ���673K��������Է�������Ϊ325�����ʣ������ʵķ���ʽΪ�� ��
��4������ʱ��FeCl3��Һ�еμ�NaOH��Һ������ҺpHΪ2.7ʱ��Fe3+��ʼ����������ҺpHΪ4ʱ��c(Fe3+)= mol/L����֪��Ksp[Fe(OH)3]= 1.1��10��36����
��5�����ռ�X��: �������������ռ�X�������ǣ� ��
��6��FeCl3����������ͨ�����õ������ⶨ����ȡmg��ˮ�Ȼ�����Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ���ݣ�ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���õ�����ָʾ������cmol/LNa2S2O3��Һ�ζ���I2+2S2O32��=2I�� +S4O62����������ȥVmL������Ʒ���Ȼ�������������Ϊ�� ��
��09�γǵ����ε��У�����X��Y��Z�����л���(����Է���������С��100)�����Ǻ�̼���⡢������4��Ԫ���е����ֻ����֡���һ����ѧϰС���ͬѧ��ȷ�����ǵ���ɻ�ṹ��
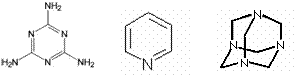
��1���ⶨ�л�����Է����������õķ���ͨ���� ������ţ���ͬ���ٺ�����ף������ף�����˴Ź����ף���
Ԫ�ط��������������ʵ���˴Ź�����ֻ��һ�����շ���ǣ�
![]()
![]()
![]()
![]()
![]()
![]() ���� �����飬 �� �� �� �� �� ��
���� �����飬 �� �� �� �� �� ��
![]()
![]() ��2��X��C��H��O��N����Ԫ����ɣ���(N)=18.67%����X���������ᷴӦ����������������Һ��Ӧ����X���ܵĽṹ��ʽΪ�� ��
��2��X��C��H��O��N����Ԫ����ɣ���(N)=18.67%����X���������ᷴӦ����������������Һ��Ӧ����X���ܵĽṹ��ʽΪ�� ��
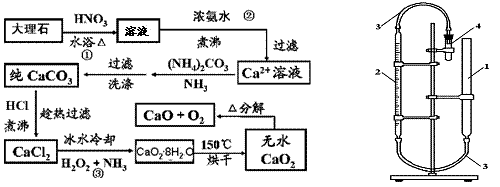
��3��Y��Z����Է���������ȣ�������ȫȼ��ʱ��ֻ������CO2��H2O��N2�е����ֻ����֡�ijͬѧȡһ������Y��Z�Ļ�����ȫȼ��ʱ�ڱ�״���µ�ʵ�������£�
ʵ����� | ����� ���� | ���ʵ�����ϵn(Y)/n(Z) | ������� | ||
m(CO2)/g | m(H2O)/g | V(N2)/mL | |||
�� | 3g | 2��3 | 3.08 | 1.8 | 672 |
�� | 3g | 3��2 | 3.52 | 1.8 | 448 |

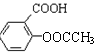 ��
��