题目内容
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同;基态b原子的核外电子占据3个能级,且最高能级轨道为半充满状态;c的最外层电子数是内层电子数的3倍;d的原子序数是c的两倍;基态e原子3d轨道上有4个单电子。
回答下列问题:
(1)b、c、d电负性最大的是___(填元素符号)。
(2)b单质分子中σ键与π键的个数比为___。
(3)a与c可形成两种二元化合物分子,两种物质可以任意比互溶。其中一种不稳定,可分解产生c的单质,该化合物分子中的c原子的杂化方式为___;这两种物质的互溶物中,存在的化学键有___(填序号)。
①极性共价键 ②非极性共价键 ③离子键 ④金属键 ⑤氢键 ⑥范德华力
(4)这些元素形成的含氧酸中,分子内中心原子的价层电子对数为4的酸是___(填化学式,下同);酸根呈正三角形结构的酸是___,试从两者结构特点判断该酸分子与酸根离子的稳定性:酸分子___酸根离子(填“>”或“<”)。
(5)元素e在周期表中的位置是___区;e的一种常见氯化物中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在,结构式为![]() ,请补写e的元素符号并用“→”表示出其中的配位键___。
,请补写e的元素符号并用“→”表示出其中的配位键___。
【答案】O 1:2 sp3 ①② H2SO4、H2SO3 HNO3 < d 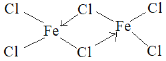
【解析】
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,a为H,基态b原子的核外电子占据3个能级,且最高能级轨道为半充满状态即2p3,则b为N,c的最外层电子数是内层电子数的3倍,则c为O,d的原子序数是c的两倍,d为S,基态e原子3d轨道上有4个单电子,则为3d6,即e为Fe。
A:H,b:N,c:O,d:S,e:Fe。
⑴电负性从左到右依次递增,从上到下依次递减,b、c、d电负性最大的是O,故答案为:O。
⑵b单质分子为氮气,氮气中σ键与π键的个数比为1:2,故答案为:1:2。
⑶a与c可形成两种二元化合物分子,分别为水和过氧化氢,过氧化氢不稳定,过氧化氢的结构式为H—O—O—H,每个氧原子有2个σ键,还有2对孤对电子,因此O原子的杂化方式为sp3,水和过氧化氢互溶物中,水中有共价键,过氧化氢中有极性共价键,非极性共价键,分子之间有范德华力和分子间氢键,但范德华力和分子间氢键不是化学键,因此存在的化学键有①②,故答案为:sp3;①②。
⑷这些元素形成的含氧酸中,有硝酸、亚硝酸、硫酸、亚硫酸,硝酸分子N有3个σ键,孤对电子为0,因此价层电子对数为3,硝酸根价层电子对数为3+0=3,为正三角形;亚硝酸分子N有2个σ键,孤对电子为1,因此价层电子对数为3,亚硝酸根价层电子对数为2+1=3,为“V”形结构;硫酸分子S有4个σ键,孤对电子为0,因此价层电子对数为4,硫酸根价层电子对数为4+0=4,为正四面体结构;亚硫酸分子S有3个σ键,孤对电子为1,因此价层电子对数为4,亚硫酸根价层电子对数为3+1=4,为三角锥形结构,因此分子内中心原子的价层电子对数为4的酸是H2SO4、H2SO3,酸根呈正三角形结构的酸是HNO3;酸分子中心原子带正电荷,吸引氧原子上的电子,使得氧与氢结合形成的电子对易断裂,因此酸分子稳定性 < 酸根离子稳定性,故答案为:H2SO4、H2SO3;HNO3;<。
⑸元素e的价电子为3d64s2,在周期表中的位置是d区,e的一种常见氯化物中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在,中间的Cl与其中易个Fe形成共价键,与另一个Fe形成配位键,Cl提供孤对电子,因此其结构式为 ,故答案为:d;
,故答案为:d; 。
。

 阅读快车系列答案
阅读快车系列答案【题目】研究与深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁。高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
温度/°C | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
则该反应的平街常数表达式K=_________,H_________0(填“>”、“<”或“=”)。
(2)CO2可用于生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
CH3OH(g)+H2O(g),为探究该反应原理,将1 mol CO2和3 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应,测得甲醇的物质的量随时间的变化如下图所示。
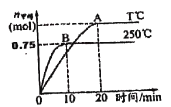
请分析并回答下列问题:
250°C时,反应在前10min的平均速率v(H2)_________molL-1min-1,从反应开始到平衡,CO2转化率为_________%。相同温度下,若某时刻该容器中含有1 mol H2、1.2mol CO2、0.8mol CH3OH、1.5 mol H2O,则此时反应所处的状态为____________________________________(填“向正反应方向进行中”、“向逆反应方向进行中心”或“平衡状态”)。