题目内容
19.在AgNO3溶液中加人铜粉和铁粉的混合物,反应完成后,向剩余固体中加稀H2SO4,无气体放出,则下列说怯正确的是( )| A. | 剩余固体一定有铜 | B. | 反应后的溶液呈蓝色 | ||
| C. | 剩余固体中一定有银 | D. | 反应后的溶液为无色 |
分析 金属银、铜、铁的活动性由强到弱的顺序铁>铜>银,在AgNO3溶液中加铜粉和铁粉的混合物,反应完成后,向剩余固体中加稀H2SO4,无气体放出,说明没有铁剩余,溶液中一定存在Fe2+,以此解答该题.
解答 解:金属银、铜、铁的活动性由强到弱的顺序铁>铜>银,在AgNO3溶液中加铜粉和铁粉的混合物,反应完成后,向剩余固体中加稀H2SO4,无气体放出,说明没有铁剩余,溶液中一定存在Fe2+,则反应后的溶液为浅绿色,不能确定铜是否参加反应,固体一定含有银,但不能确定是否含有铜,溶液不一定呈蓝色,只有C正确.
故选C.
点评 本题综合考查元素化合物知识,为高频考点,侧重于学生的分析能力的考查,注意把握金属的活泼性,难度不大.

练习册系列答案
相关题目
9.下列各组物质,互为同系物的是( )
| A. | CH3-CH=CH2与 | B. |  与 与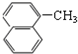 | ||
| C. |  与 与 | D. | CH3CH2Cl与CH3CHCl-CH2Cl |
10.在两个容积相同的容器中,一个盛有C2H4气体,另一个盛有N2和CO的混合气体.在同温同压下,两容器内的气体一定相同的物理量有几项( )
(1)分子数 (2)原子数 (3)质量 (4)电子数 (5)密度 (6)摩尔质量 (7)气体摩尔体积.
(1)分子数 (2)原子数 (3)质量 (4)电子数 (5)密度 (6)摩尔质量 (7)气体摩尔体积.
| A. | 4项 | B. | 5项 | C. | 6项 | D. | 7项 |
14.已知CuO经高温灼烧生成Cu2O,Cu2O与H+发生:Cu2O+2H+═Cu+Cu2++H2O.将经高温灼烧后的CuO样品投入足量的热的稀硝酸溶液中,下列有关说法中正确的是( )
| A. | 如果溶液变为蓝色,同时有紫红色固体出现,说明样品全部生成了Cu2O | |
| B. | 溶液中最终可能有紫红色固体出现 | |
| C. | 这种实验的结果无法说明CuO分解的程度 | |
| D. | 如果溶液中出现蓝色,最终没有紫红色固体出现,说明CuO没有分解 |
4.下列方程式中电子转移数目正确的是( )
| A. | 3NO2+H20═2HNO3+NO,转移3e- | |
| B. | 2KMnO4+10FeSO4+8H2SO4═K2SO4+5Fe2(SO4)3+2MnSO4+8H20,转移5e- | |
| C. | KClO3+6HCl═KCl+3Cl2↑+3H20,转移6e- | |
| D. | I2+SO2+2H20═H2SO4+2HI,转移2e- |
11.在反应3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中,氧化剂与还原剂的质量之比是( )
| A. | 3:8 | B. | 32:21 | C. | 21:32 | D. | 21:8 |
12.将等物质的量的A、B混合于1L的密闭容器中,发生反应:2A(g)+B(g)?2C(g)+D(?),5min时,测得密闭容器内气体压强减小,且c(A):c(B)=3:4,5min内,v(A)=0.2mol•L-1•minL-1,下列有关结论正确的是( )
| A. | D为气体 | B. | B的转化率为80% | ||
| C. | 5min时,c(A)=1.5mol•L-1 | D. | 反应开始前A的物质的量为2mol |
13.下列有关实验装置进行的相应实验,能达到实验目的是( )


| A. | 用图1所示装置除去HCl中含有的少量Cl2 | |
| B. | 用图2所示装置将硫酸铜溶液蒸干,制备胆矾 | |
| C. | 用图3所示装置可以完成“喷泉”实验 | |
| D. | 用图4所示装置制取并收集干燥纯净的NH3 |