题目内容
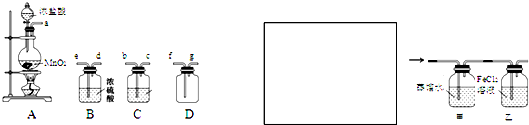
某化学小组用下列装置抽取收集纯净的氯气,并研究其性质。请回稳下列问题。

(1)装置A中发生反应的离子方程式为_______________________________。
(2)按照气流方向各仪器接口的连接顺序为a→___________________→g。
(3)装置B中浓硫酸的作用是__________________________,装置C的试剂最好是___________________________________。
(4)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。
|
|
(5)装制取的氯气通入下图所示装置中,甲装置溶液中具有氧化性的含氯粒子是_______;如何证明乙装置中FeCl2溶液与Cl2发生了反应?(只回答需要的试剂和现象)_ 。

(1)MnO2+4H+ +2Cl-  Mn2++Cl2 ↑+ 2H2O
Mn2++Cl2 ↑+ 2H2O
(2)bcedf
(3)吸收水蒸气,干燥氯气,饱和食盐水
(4)
(5)Cl2 、HClO、ClO- ,KSCN溶液,溶液变成血红色
【解析】
试题分析:(1)实验室制取氯气使用MnO2和浓盐酸。(2)先除去HCl杂质,再除去H2O杂质,最后收集。
(3)浓硫酸起到干燥的作用,除去HCl气体杂质使用饱和食盐水。(4)尾气吸收使用NaOH溶液。(5)Fe2+被氯气氧化为Fe3+ ,检验Fe3+使用KSCN溶液,溶液变成血红色。
考点:考察实验室制取氯气的原理和操作。能正确的处理除杂和尾气吸收。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案某化学小组用下列装置抽取收集纯净的氯气,并研究其性质。请回稳下列问题。

(1)装置A中发生反应的离子方程式为_______________________________。
(2)按照气流方向各仪器接口的连接顺序为a→___________________→g。
(3)装置B中浓硫酸的作用是____________________________________________________________,装置C的试剂最好是___________________________________。
(4)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。
|
|
(5)装制取的氯气通入下图所示装置中,甲装置溶液中具有氧化性的含氯粒子是_______;如何证明乙装置中FeCl2溶液与Cl2发生了反应?(只回答需要的试剂和现象)___________________________。