题目内容
已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40 kJ的热量。表示上述反应的热化学方程式正确的是…( )A.C8H18(l)+![]() O2(g)
O2(g)![]() 8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
B.C8H18(l)+![]() O2(g)
O2(g)![]() 8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
C.C8H18(l)+![]() O2(g)
O2(g)![]() 8CO2(g)+9H2O ΔH=+5 518 kJ·mol-1
8CO2(g)+9H2O ΔH=+5 518 kJ·mol-1
D.C8H18(l)+ ![]() O2(g)
O2(g)![]() 8CO2(g)+9H2O(l) ΔH=-48.40 kJ·mol-1
8CO2(g)+9H2O(l) ΔH=-48.40 kJ·mol-1
解析:在25 ℃、101 kPa下,1 mol C8H18燃烧生成CO2和液态水时放出的热量为![]() ×114g=5 518 kJ。由于在判断热化学方程式时应注明以下几点:①标明各物质的状态,A中H2O的状态标错,A不正确;②标明反应是吸热还是放热,ΔH>0时为吸热反应,ΔH<0时为放热反应,C错;③热量数值要与化学计量数相对应,显然D错。
×114g=5 518 kJ。由于在判断热化学方程式时应注明以下几点:①标明各物质的状态,A中H2O的状态标错,A不正确;②标明反应是吸热还是放热,ΔH>0时为吸热反应,ΔH<0时为放热反应,C错;③热量数值要与化学计量数相对应,显然D错。
答案:B

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
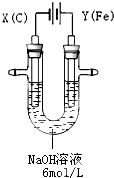 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.