��Ŀ����
6�� ��˾ƥ�֣��ֳ�����ˮ���ᣬ
��˾ƥ�֣��ֳ�����ˮ���ᣬ ��������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128-135�森ijѧϰС����ʵפ����ˮ���ᣨ���ǻ������ᣩ��������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣����Ʊ�ԭ��Ϊ��
��������Ӧ����㷺�Ľ��ȡ���ʹ�Ϳ���ҩ������ˮ���������ֽ⣬�ֽ��¶�Ϊ128-135�森ijѧϰС����ʵפ����ˮ���ᣨ���ǻ������ᣩ��������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣����Ʊ�ԭ��Ϊ��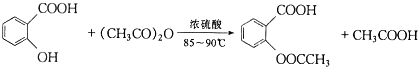
�Ʊ������������̡�װ��ʾ��ͼ���й��������£��гֺͼ�����������ȥ����
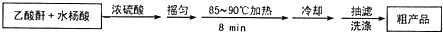
�����������Ϣ�ش��������⣺
��1���Ʊ�����˾ƥ��ʱ��Ҫʹ�ø���������ԭ������������ˮ��Ӧ��
��2���ϳɰ�˾ƥ��ʱ������ʵļ��ȷ�����ˮԡ���ȣ���ԭ���DZ��ڿ����¶ȣ���ֹ����ˮ���������ֽ⣮�������ôֲ�ƷҪ��������ˮϴ�ӣ���Ŀ���dz�ȥ�����������ᡢ���ᣬ��������ˮ������ˮ�е��ܽ⣮
��3���������ôֲ�Ʒ�л���һЩ����Ʒ��������һ���Ǹ߷��ӻ�����ᴿ�ֲ�Ʒ��

�������ᴿ���������ؽᾧ����
�ڸ÷�����ѡ�������������ܼ���ԭ����ˮ���ᡢ����ˮ���ᶼ����ˮ���߷��ӻ����ﲻ����ˮ����ˮ���ܼ����ܷ��룬��ˮ������������������������ˮ������ܣ��߷��ӻ����ﲻ�����������������˷�����߷��ӻ����ͨ���ؽᾧ���Եõ�����ˮ���ᣮ
��4����ѧϰС����ʵ����ԭ��������2.0gˮ���ᡢ5.0mL����������=1.08g•cm-3 �������ճƵò�Ʒ����m=2.2g������������ˮ����IJ���Ϊ84.3%���������3λ��Ч���֣���
���� ��1��������������ˮ��Ӧ����ˮ�ⷴӦ���Ʊ�������Ӧ���
��2�������¶���85�桫90�棬�¶ȵ���100�棬Ӧ��ȡˮԡ���ȣ����ڿ����¶ȣ���ֹ����ˮ���������ֽ⣻
��Ʒ�ḽ�������������ᡢ���ᣬ��Ҫϴ�ӳ�ȥ����ˮ���Խ���Ӧ�ܽ�µ���ʧ��
��3�������ᴿ����ͼ����֪�����ø߷��ӻ����ˮ����������ˮ���������������е��ܽ�Ȳ�ͬ���з��룻
��ˮ���ᡢ����ˮ���ᶼ����ˮ���߷��ӻ����ﲻ����ˮ����ˮ���ܼ����ܷ��룬��ˮ������������������������ˮ������ܣ��߷��ӻ����ﲻ�����������������˷�����߷��ӻ��������ȴ�ᾧʱ��ˮ�����ܽ������������У����ٽᾧ������
��4������ˮ���ᡢ�����������ʵ��������й����жϣ����ݲ����������ʼ������۲���������������ʣ�
��� �⣺��1��������������ˮ���������ᣬ������Ӧ�����ֹ������ˮ�⣬
�ʴ�Ϊ����������ˮ��Ӧ��
��2�������¶���85�桫90�棬�¶ȵ���100�棬Ӧ��ȡˮԡ���ȣ����ڿ����¶ȣ���ֹ����ˮ���������ֽ⣻
��Ʒ�ḽ�������������ᡢ���ᣬ��Ҫϴ�ӳ�ȥ����ˮ���Խ�������ˮ������ˮ�е��ܽ⣬������ʧ��
�ʴ�Ϊ��ˮԡ���ȣ����ڿ����¶ȣ���ֹ����ˮ���������ֽ⣻��ȥ�����������ᡢ���ᣬ��������ˮ������ˮ�е��ܽ⣻
��3�������ᴿ����ͼ����֪�����ø߷��ӻ����ˮ����������ˮ���������������е��ܽ�Ȳ�ͬ���з��룬���ַ����ᴿ����Ϊ�ؽᾧ���ʴ�Ϊ���ؽᾧ����
��ˮ���ᡢ����ˮ���ᶼ����ˮ���߷��ӻ����ﲻ����ˮ����ˮ���ܼ����ܷ��룬��ˮ������������������������ˮ������ܣ��߷��ӻ����ﲻ�����������������˷�����߷��ӻ��������ȴ�ᾧʱ��ˮ�����ܽ������������У����ٽᾧ������ͨ���ؽᾧ���Եõ�����ˮ���ᣬ��ѡ�������������ܼ���
�ʴ�Ϊ��ˮ���ᡢ����ˮ���ᶼ����ˮ���߷��ӻ����ﲻ����ˮ����ˮ���ܼ����ܷ��룬��ˮ������������������������ˮ������ܣ��߷��ӻ����ﲻ�����������������˷�����߷��ӻ����ͨ���ؽᾧ���Եõ�����ˮ���
��4��ˮ�������Է�������Ϊ138��n��ˮ���ᣩ=2.0 g��138g/mol=0.0145mol��n����������=��5.0 mL��1.08 g/cm3����102g/mol=0.0529mol�����������������ʵ�������ˮ���ᣬ���Եõ�������ˮ����Ӧ�ð���ˮ���������㣬�������ϵõ�����ˮ���������Ϊ0.0145mol��180g/mol=2.61g����������ˮ����IJ���Ϊ��2.2g��2.61g����100%=84.3%��
�ʴ�Ϊ��84.3%��
���� ���⿼���л����Ʊ�ʵ�鷽����������ۣ���3����ע�����������������ᴿ�������ϺõĿ���ѧ����������������������Ŀ�Ѷ��еȣ�

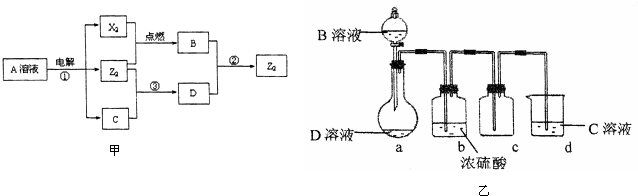
 ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�| A�� | 4Fe+3O2�T2Fe2O3 | B�� | O2+4e-+2H2O�T4OH- | ||
| C�� | 4Fe��OH��2+O2+2H2O�T4Fe��OH��3 | D�� | Fe+2H+�TFe2++H2�� |
| A�� | ����������ȵ͵�ֲ�������������������ʹˮ�ֽ�����������÷���������ɫ��ѧԭ�� | |
| B�� | 12C��13C��14C��Ϊͬλ�أ����ǵķ����Կ����ڿ��Ŷϴ����ɲⶨ��������������� | |
| C�� | ���߷ֱ�ӫ���������Թ۲쵽�������磬����������ӫ�⵰�ף������Ҳ��ӫ�⵰���йأ�������ǽ���ѧ��ת��Ϊ���ܵĹ��� | |
| D�� | ����ɸ����������״��Ѩ��ͨ�������ڷ��롢�ᴿ���壬������������������ӽ������������ʹ������� |
| A�� | pH=1����Һ��Na+��Fe3+��SO${\;}_{4}^{2-}$��NO${\;}_{3}^{-}$ | |
| B�� | ������ȳʺ�ɫ����Һ�У�K+��HCO${\;}_{3}^{-}$��Cl-��CO${\;}_{3}^{2-}$ | |
| C�� | c��OH-��=1.0��10-13mol•L-1����Һ�У�SO${\;}_{3}^{2-}$��SiO${\;}_{3}^{2-}$��NO${\;}_{3}^{-}$��K+ | |
| D�� | c��I-��=0.1 mol•L-1����Һ�У�Na+��NH${\;}_{4}^{+}$��ClO-��SO${\;}_{4}^{2-}$ |
 ����ˮ��������߳��ĵ����þƬ������̿Ϊ�缫�����ϵμ�ʳ��ˮ���ر�ɹ�������ط�ӦΪ2Mg+O2+2H2O=2Mg��OH��2�����й��ڸõ�ص�˵��������ǣ�������
����ˮ��������߳��ĵ����þƬ������̿Ϊ�缫�����ϵμ�ʳ��ˮ���ر�ɹ�������ط�ӦΪ2Mg+O2+2H2O=2Mg��OH��2�����й��ڸõ�ص�˵��������ǣ�������| A�� | þƬ��Ϊ���� | |
| B�� | ʳ��ˮ��Ϊ�������Һ | |
| C�� | ��ع���ʱþƬ������ | |
| D�� | ��ع���ʱʵ���˻�ѧ������ܵ�ת�� |
| A�� | ���ü��ȷֽⷨұ�������� | B�� | ���õ�ⷨұ������������ | ||
| C�� | �����Ȼ�ԭ��ұ���������빯 | D�� | �����Ȼ�ԭ��ұ������ͭ��� |