题目内容
1mol?L-1NaOH溶液的含义是( )
| A、1L水中有1molNaOH |
| B、溶液中有1molNaOH |
| C、1L溶液中含有40克NaOH |
| D、将40克NaOH溶于1L水中所得的溶液 |
考点:物质的量浓度
专题:化学用语专题
分析:物质的量浓度概念为:单位体积溶液中含有溶质的物质的量,即cB=
,1mol/L NaOH溶液的含义是:1LNaOH溶液中含有溶质NaOH的物质的量为1mol,据此进行分析即可.
| n B |
| V |
解答:
解:A、1 L溶液中含有1mol NaOH,不是1L水中含有1molNaOH,故A错误;
B、必须指出溶液的体积,1mol/L NaOH溶液的含义为1LNaOH溶液中含有溶质NaOH的物质的量为1mol,故B错误;
C、1mol/L NaOH溶液的含义为1LNaOH溶液中含有溶质NaOH的物质的量为1mol,质量为40g,故C正确;
D、40g氢氧化钠溶于1L水中,得到的溶液的体积不是1L,无法计算溶液的浓度,故D错误;
故选C.
B、必须指出溶液的体积,1mol/L NaOH溶液的含义为1LNaOH溶液中含有溶质NaOH的物质的量为1mol,故B错误;
C、1mol/L NaOH溶液的含义为1LNaOH溶液中含有溶质NaOH的物质的量为1mol,质量为40g,故C正确;
D、40g氢氧化钠溶于1L水中,得到的溶液的体积不是1L,无法计算溶液的浓度,故D错误;
故选C.
点评:本题考查了物质的量浓度,题目难度不大,侧重了基础知识的考查,旨在检查学生对物质的量浓度概念的理解情况.

练习册系列答案
相关题目
在0.5L某浓度的Na2SO4溶液中含有0.5mol Na+,下列对该溶液的说法中,正确的是( )
| A、该溶液的物质的量浓度为1mol?L-1 |
| B、该溶液中含有71g Na2SO4 |
| C、配制100mL该溶液需用7.1g Na2SO4 |
| D、量取100mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.2mol |
下列说法正确的是( )
| A、乙烯和聚氯乙烯都能发生加成反应 |
| B、CuSO4溶液能使鸡蛋清盐析而沉淀 |
| C、乙酸、乙醇和乙酸乙酯可用饱和Na2CO3溶液鉴别 |
| D、浓HNO3不能与苯发生取代反应 |
下列说法正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 |
| B、△H<0,△S<0的反应在任何温度下自发进行 |
| C、同一种物质不同状态时熵值大小为S(g)<S(l)<S(s) |
| D、反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
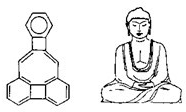 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛(如图).因而称为释迦牟尼分子(所有原子在同一平面).有关该有机分子的说法不正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有22个碳原子 |
| D、该有机物可发生加成反应 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.3mol/L NaCl溶液含离子总数为0.6NA |
| B、常温常压下,18g H2O中含有的电子数总数为10NA |
| C、标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA |
| D、1L 2 mol/L Na2CO3溶液中含有的CO32-数目为4NA |
下列叙述中,正确的是( )
| A、一个基态多电子的原子中,可以有运动状态完全相同的电子 |
| B、元素原子的最外层电子数等于元素的最高正价 |
| C、凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体 |
| D、电子构型为[Ar]3d54s2的元素是过渡元素 |
下列各组溶液中离子,能在溶液中大量共存的是( )
| A、H+、Ca2+、NO3-、CO32- |
| B、K+、Na+、Cl-、NO3- |
| C、Ag+、Na+、Cl-、K+ |
| D、NH4+、K+、NO3-、SO42- |
反应NH4HS(s)?NH3(g)+H2S(g),在某一温度下达到平衡.下列各种情况中,不能使化学平衡发生移动的是( )
| A、其他条件不变时通入SO2气体 |
| B、移走一部分NH4HS固体 |
| C、容器体积不变,充入N2 |
| D、压强不变时,充入N2 |