题目内容
12.在5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2+9H2O反应中,氧化剂与还原剂物质的量之比是( )| A. | 5:8 | B. | 5:4 | C. | 5:3 | D. | 3:5 |
分析 在氧化还原反应5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2+9H2O中,-3价的N元素的化合价升高,被氧化,做还原剂;+5价N元素的化合价降低,被还原,做氧化剂,据此判断氧化剂与还原剂的物质的量之比.
解答 解:在氧化还原反应5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2+9H2O中,-3价的N元素的化合价升高,被氧化,做还原剂;+5价N元素的化合价降低,被还原,做氧化剂,
其中有$\frac{2}{5}$的+5价N,没有变价,所以该反应中氧化剂与还原剂的物质的量之比是3:5,
故选D.
点评 本题考查了氧化还原反应的计算,题目难度中等,正确判断还原剂的量为解答关键,注意熟练掌握氧化剂、还原剂的概念及判断方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的物质的量比乙的物质的量小 | |
| C. | 气体摩尔体积:甲<乙 | |
| D. | 甲的相对分子质量比乙的相对分子质量小 |
7.某元素的第一电离能至第七电离能(KJ/mol)如下:
该元素最有可能位于元素周期表的族是( )
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
| A. | ⅠA | B. | ⅡA | C. | ⅢA | D. | ⅣA |


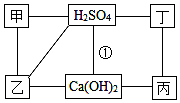 如图中的每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.
如图中的每条连线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种.