题目内容
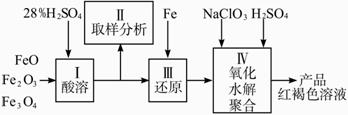
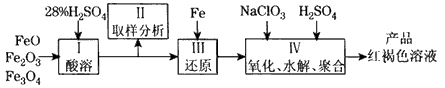
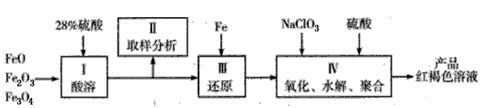
硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理.用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+.

实验步骤如下:
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有________.
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是________.
a.控制溶液中Fe2+与Fe3+含量比
b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量
d.确保铁的氧化物酸溶完全
(3)用NaClO3氧化时反应方程式如下:
6FeSO4+NaClO3+3H2SO4![]() 3Fe2(SO4)3+NaCl+3H2O
3Fe2(SO4)3+NaCl+3H2O
若改用HNO3氧化,则反应方程式如下
6FeSO4+2HNO3+3H2SO4![]() 3Fe2(SO4)3+2NO↑+4H2O
3Fe2(SO4)3+2NO↑+4H2O
已知1 mol HNO3价格0.16元、1 mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的利弊,利是________,弊是________.
(4)聚合硫酸铁溶液中![]() 与Fe3+物质的量之比不是3∶2.根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2.根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中![]() 与Fe3+物质的量之比.
与Fe3+物质的量之比.
测定时所需的试剂________.
a.NaOH b.FeSO4
c.BaCl2 d.NaClO3
(5)需要测定________和________的质量.(填写化合物的化学式)
(6)选出测定过程中所需的基本操作________(按操作先后顺序列出).
a.萃取、分液
b.过滤、洗涤
c.蒸发、结晶
d.冷却、称量
e.烘干或灼烧
解析:
|
答案:(1)b (2)bc (3)原料成本较低 产生气体对大气有污染 (4)ac (5)Fe2O3 BaSO4 (6)bed 思路解析:配制一定物质的量浓度的溶液时通常需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和容量瓶等. |

 名校课堂系列答案
名校课堂系列答案
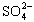 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中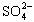 与Fe3+物质的量之比。?
与Fe3+物质的量之比。?