题目内容
6.0 g某有机物A完全燃烧后,生成标况下的CO2 6.72 L和7.2 g H2O,测得该化合物的蒸气对氢气的相对密度是30,求该化合物的分子式。
【答案】
C3H8O
【解析】考查有机物分子式判断
化合物的蒸气对氢气的相对密度是30
所以该有机物的相对分子质量是30×2=60
因此6.0 g有机物A的物质的量是0.1mol
生成的CO2和水的物质的量分别是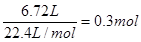 、
、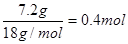
所以根据原子守恒可知有机物中碳、氢原子的个数分别是3和8
因此氧原子的个数是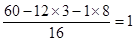
所以有机物的分子式为C3H8O。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目