题目内容
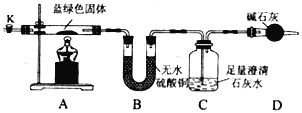
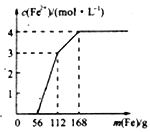
【题目】某化学兴趣小组利用还原铁粉处理含Fe(NO3)3、Cu(NO3)2、HNO3的废水,所加还原铁粉的质量与溶液中Fe2+的浓度变化关系如下图(忽略溶液体积变化)。下列有关结论错误的是( )
A. 加入铁粉质量小于56g时发生的反应为Fe+NO3-+4H+=Fe3++NO↑+2H2O
B. 当加入的铁粉质量超过168g后,溶液中的溶质只含有Fe(NO3)2(忽略Fe2+的水解)
C. 原废水中Fe(NO3)3的浓度为2mol/L,Cu(NO3)2的浓度均为1mol/L
D. 原废水中三种物质的氧化性由强到弱的顺序是HNO3>Fe(NO3)3>Cu(NO3)2
【答案】C
【解析】刚开始加入56g(1mol)单质铁,溶液中不生成Fe2+,所以发生的化学反应一定是铁被硝酸氧化为Fe3+。其方程式为:Fe+NO3-+4H+=Fe3++NO↑+2H2O。选项A正确。当加入的单质铁完全过量的时候,溶液中的Fe(NO3)3、Cu(NO3)2、HNO3应该都被反应为Fe(NO3)2,选项B正确。56g至112g(1mol)间加入1molFe,Fe2+的浓度增加3mol/L,而112g至168g(1mol)间加入1molFe,Fe2+的浓度增加1mol/L,所以说明前一个1molFe发生的是Fe + 2Fe3+ =3Fe2+,后一个1mol反应为Fe + Cu2+ =Fe2+ + Cu,将反应物均为1molFe带入计算,得到Fe(NO3)3浓度为2mol/L,Cu(NO3)2的浓度为1mol/L,但是考虑到第一步中加入的1molFe和硝酸反应得到了1mol/L的Fe(NO3)3,所以原废水中Fe(NO3)3浓度为1mol/L,选项C错误。因为废水中三种物质和单质铁反应的顺序是HNO3、Fe(NO3)3、Cu(NO3)2,反应中应该是氧化性强的物质先反应,所以氧化性为:HNO3>Fe(NO3)3>Cu(NO3)2。选项D正确。

 天天向上口算本系列答案
天天向上口算本系列答案【题目】海洋是“聚宝盆”,工业上,人们直接从海水中得到食盐。海水在浓缩过程中析出盐类物质的种类和质量,如下表:
海水密度(g/L) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.13 | 0.56 | ||||
1.20 | 0.91 | ||||
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
(1)常采用____________的方法从海水中得到食盐。
(2)为得到含杂质较少的食盐,实际生产中卤水的密度控制在_____之间。
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,通常在实验室中依次加入_________、__________、___________、___________等四种物质除去杂质。(填化学式)
(4)电解饱和食盐水可以制取氯气,同时得到几种重要的化工产品,
该反应的化学方程式为_________________________________________。通电时阳极产物是__________该产物的检验方法是___________________________________________
(5)电解过程中得到气体物质还可以化合为HCl,在实验室中我们利用_________________和_____________ 反应(写名称)来制取。该气体__________________溶于水,可以做喷泉实验。写出氯化氢气体溶于水后的电离方程式_____________________________________
(6)新制的氯水显_______色,这是因为氯水中有__________(填微粒符号)存在。向氯水中滴入几滴AgNO3溶液,观察到的现象是____________________________,发生变化的化学方程式为______________________________________________。蓝色石蕊试纸遇到氯水后的现象是___________________________,氯气有毒,不能直接排放到空气中,需要用________________________来吸收,写出反应的化学方程式为_________________________________________