题目内容
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题:
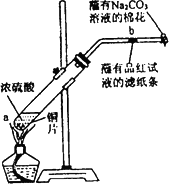
(1)写出a处反应的化学方程式________.
(2)试管中的液体反应一段时间后,b处滤纸条的变化为________.待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为________.
(3)待试管中液体冷却后,将试管上层液体倒去,再慢慢加入少量水,可观察溶液呈________色.
(4)玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是________
(5)如果浓硫酸的浓度为18 mol/L,铜片是过量的,加热使之反应,当被还原的硫酸为0.9 mol.则浓硫酸的实际体积________(填写“大于”、“等于”或“小于”)100 mL.
答案:
解析:
解析:
|
(1)Cu+2H2SO4(浓)=CuSO4+SO2+H2O. (2)滤纸颜色褪去.滤纸颜色恢复. (3)蓝色. (4)吸收产生的SO2,防止大气污染 (5)大于 |

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
 某学生做浓硫酸性质的实验:
某学生做浓硫酸性质的实验: 在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题:
在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上.把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中.塞紧试管口,在玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花.给试管加热,观察现象.当试管中的液体逐渐透明时,停止加热.回答下列问题:


