题目内容
11.根据下列实验操作和现象,所得结论正确的是( )| 实验操作、现象 | 结 论 | |
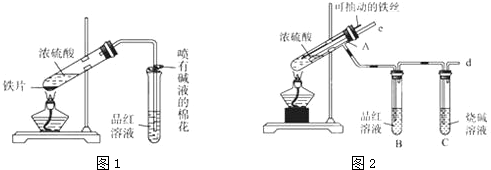
| A | 火柴梗上滴少量的浓硫酸;火柴梗变黑 | 浓硫酸具有强氧化性 |
| B | 含锈的铁浸泡在NH4Cl溶液中,铁锈逐渐溶解 | NH4Cl显酸性 |
| C | Ba(NO3)2溶液中通入SO2气体;产生白色沉淀 | BaSO3难溶 |
| D | 某无色溶液中通入过量的CO2气体,有白色沉淀 | 一定含有AlO2- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.火柴梗变黑,使H、O以水的形式脱出,只留下C;
B.NH4Cl溶液水解显酸性,与含锈的铁反应;
C.Ba(NO3)2溶液中通入SO2气体,发生氧化还原反应生成硫酸钡沉淀;
D.无色溶液中通入过量的CO2气体,有白色沉淀,白色沉淀为氢氧化铝和硅酸.
解答 解:A.火柴梗变黑,使H、O以水的形式脱出,只留下C,体系浓硫酸的脱水性,与强氧化性无关,故A错误;
B.NH4Cl溶液水解显酸性,与含锈的铁反应,则铁锈逐渐溶解,故B正确;
C.Ba(NO3)2溶液中通入SO2气体,发生氧化还原反应生成硫酸钡沉淀,结论不合理,故C错误;
D.无色溶液中通入过量的CO2气体,有白色沉淀,白色沉淀为氢氧化铝和硅酸,可能含有AlO2-,结论不合理,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生反应和现象为解答本题关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
1.已知298 K,101kPa时,2SO2(g)+O2(g)???2SO3(g)△H=-197kJ•mol-1.在相同温度和压强下,向密闭容器中通入2mol SO2和1mol O2,达到平衡时,放出热量为Q1,向另一个体积相同的容器中通入1mol SO2,0.5mol O2 和1mol SO3,达到平衡时放出热量为Q2,则下列关系正确的是( )
| A. | Q2<Q1<197 kJ•mol-1 | B. | Q2=Q1=197 kJ•mol-1 | ||
| C. | Q1<Q2<197 kJ•mol-1 | D. | Q2=Q1<197 kJ•mol-1 |
2.下列有关化学反应的说法正确的是( )
| A. | 在氧化还原反应中,阴离子只能发生氧化反应 | |
| B. | 碳酸钠溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 有些吸热反应不需要加热也能进行 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
19.一定条件下,碳单质和二氧化碳气体可以反应生成一氧化碳气体,该反应的类型为( )
| A. | 吸热反应 | B. | 离子反应 | C. | 复分解反应 | D. | 非氧化还原反应 |
6.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )
| A. | 电子由Zn电极流出,经KOH溶液流向正极 | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
16.下列离子方程式正确的是( )
| A. | 少量金属钠投入水中:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 60 mL 1 mol/L纯碱溶液与20 mL 2 mol/L胆矾溶液混合(无气体放出):3CO32-+2Cu2++2H2O=2HCO3-+Cu2(OH)2CO3↓ | |
| C. | 向H2O中投入少量Na218O2固体:2H2O+2Na218O2=4Na++418OH-+O2↑ | |
| D. | 向碳酸氢钙溶液中加入少量KOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
20.下列各组离子中,能在溶液中大量共存的是( )
| A. | H+、Ca2+、Cl-、CO32- | B. | Cl-、ClO-、K+、H+ | ||
| C. | Na+、Fe3+、SO42-、OH- | D. | Na+、Cu2+、Cl-、SO42- |

 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +CO2↑
+CO2↑ $→_{△}^{NaOH(aq)}$
$→_{△}^{NaOH(aq)}$ +H2O
+H2O $→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
$→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
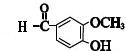 +CH3COCH2COCH3$→_{△}^{NaOH(aq)}$
+CH3COCH2COCH3$→_{△}^{NaOH(aq)}$ +2H2O.
+2H2O.