题目内容
已知下列各组反应,对应的离子方程式正确的是
- A.钠与水反应:Na+H2O=Na++OH-+H2↑
- B.氯气和氯化亚铁反应:Cl2+Fe2+=2Cl-+Fe3+
- C.铝与硝酸铜反应:Al+Cu2+=Cu+Al3+
- D.FeCl3溶液与铜单质反应:2Fe3++Cu=Cu2++2Fe2+
D
在判断离子方程式的正误时,看离子方程式是否反映了化学反应的实质;看物质化学式的拆分是否正确;三看离子方程式是否符合“三个守恒”。 A中违背了质量守恒定律和电子转移守恒,应为:2Na+2H2O=2Na++2OH-+H2↑。B中违背了电荷守恒和电子得失守恒,Cl2+2Fe2+=2Cl-+2Fe3+。C中电荷不守恒,电子丢失不守恒。应为:2Al+3Cu2+=3Cu+2Al3+。D正确。
在判断离子方程式的正误时,看离子方程式是否反映了化学反应的实质;看物质化学式的拆分是否正确;三看离子方程式是否符合“三个守恒”。 A中违背了质量守恒定律和电子转移守恒,应为:2Na+2H2O=2Na++2OH-+H2↑。B中违背了电荷守恒和电子得失守恒,Cl2+2Fe2+=2Cl-+2Fe3+。C中电荷不守恒,电子丢失不守恒。应为:2Al+3Cu2+=3Cu+2Al3+。D正确。

练习册系列答案
相关题目
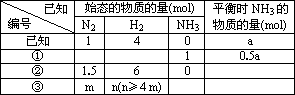
(7分)在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2⇌2NH3已知加入1 mol N2、4 mol H2时,达到平衡后生成a mol NH3(见表中已知项),在相同温度和压强下保持平衡后各组分体积分数不变,对下列编号①~③的状态,填写表中空白。
| 已知编号 | 始态的物质的量(mol) | 平衡时NH3的 物质的量(mol) | ||
| N2 | H2 | NH3 | ||
| 已知 | 1 | 4 | 0 | a |
| ① |
|
| 1 | 0.5a |
| ② | 1.5 | 6 | 0 |
|
| ③ | m | n( n≥4m) |
|
|
(7分)在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2⇌2NH3已知加入1 mol N2、4 mol H2时,达到平衡后生成a mol NH3(见表中已知项),在相同温度和压强下保持平衡后各组分体积分数不变,对下列编号①~③的状态,填写表中空白。
|
已知编号 |
始态的物质的量(mol) |
平衡时NH3的 物质的量(mol) |
||
|
N2 |
H2 |
NH3 |
||
|
已知 |
1 |
4 |
0 |
a |
|
① |
|
|
1 |
0.5a |
|
② |
1.5 |
6 |
0 |
|
|
③ |
m |
n( n≥4m) |
|
|