题目内容
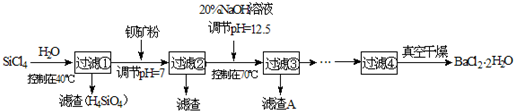
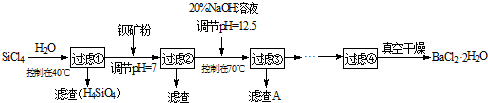
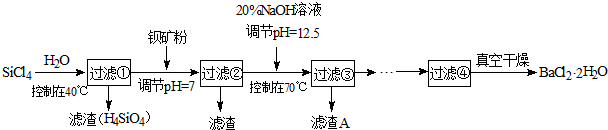
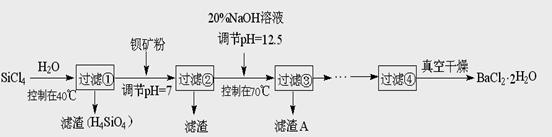
(12分)多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它对环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,且含有钙、铁、镁等离子)制备BaCl2·2H2O,工艺流程如下。已知常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。
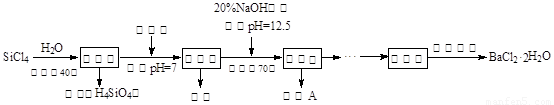
(1)SiCl4水解控制在40℃以下的原因是 ▲ 。
已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g) ΔH1=47 kJ/mol
SiHCl3(s)+H2(g)=Si(s)+3HCl(g) ΔH2=189 kJ/mol
则由SiCl4制备硅的热化学方程式为 ▲ 。
(2)加钡矿粉时生成BaCl2的离子反应方程式是 ▲ 。
(3)加20% NaOH调节pH=12.5,得到滤渣A的主要成分是 ▲ ,控制温度70℃的目的是 ▲ 。
(4)BaCl2滤液经蒸发浓缩、降温结晶、过滤,再经真空干燥后得到·2H2O。实验室中蒸发浓缩用到的含硅酸盐的仪器有 ▲ 种。
(5)为体现该工艺的绿色化学思想,该工艺中能循环利用的物质是 ▲ 。
【答案】
(1)防止HCl挥发污染环境或控制SiCl4的水解速率,防止反应过于剧烈。SiCl4(s)+2H2(g)=Si(s)+4HCl(g) ΔH=236kJ/mol(4分)
(2)BaCO3+2H+=Ba2++CO2+H2O↑(2分)
(3)Mg(OH)2、Ca(OH)2,
确保钙离子完全除去(或温度越高,Ca(OH)2溶解度越小)。(2分)
(4)3(2分)
(5)BaCl2溶液(2分)
【解析】

练习册系列答案
相关题目