题目内容
17.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 5.6 g金属铁与足量的稀硫酸反应失去的电子数为0.3NA | |
| B. | 常温常压下,22.4L O2中含有氧原子个数为2NA | |
| C. | 2.8 g CO与等质量的C2H4含有相等的分子数,都为0.1NA | |
| D. | 1 mol•L-1NaCl溶液中含有Cl-的个数为NA |
分析 A、求出铁的物质的量,然后根据铁与稀硫酸反应后变为+2价来分析;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、CO与等质量的C2H4的摩尔质量均为28g/mol;
D、溶液体积不明确.
解答 解:A、5.6g铁的物质的量为0.1mol,而铁与稀硫酸反应后变为+2价,故0.1mol铁失去0.2mol电子,即0.2NA个,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L氧气的物质的量小于1mol,故氧原子的物质的量小于2mol,小于2NA个,故B错误;
C、CO与等质量的C2H4的摩尔质量均为28g/mol,故2.8gCO和2.8gC2H4的物质的量均为0.1mol,分子数均为0.1NA个,故C正确;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.已知:在同一反应中,氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性.在一定条件下KClO3与I2按下式反应:2KClO3+I2═2KIO3+Cl2,下列判断正确的是( )
| A. | 该反应属于置换反应 | B. | 还原剂为KClO3,氧化剂为I2 | ||
| C. | 还原性:I2>KIO3 | D. | 氧化性:KClO3>KIO3 |
5.下列属于同位素的一组是( )
| A. | O2、O3 | B. | H2O、D2O | C. | H、D | D. | 1944K、2040Ca |
12.下列电子式书写不正确的是( )
| A. | 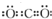 | B. | 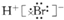 | C. | 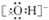 | D. | 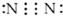 |
2.下列说法中正确的是( )
| A. | 铝在空气中耐腐蚀,所以铝是不活泼金属 | |
| B. | 点燃的镁条插入盛有二氧化碳的集气瓶里,则迅速熄灭 | |
| C. | 铝在高温下能还原锰、铁、铬等金属的氧化物 | |
| D. | 因为镁和铝在空气中都能形成氧化膜,所以镁和铝都不溶于浓硝酸 |
6.利用右图实验装置,能得出相应实验结论的是( )
| ① | ② | ③ | 实验结论 |  | |
| A | 浓醋酸 | CaCO3 | Ca(ClO)2 | 酸性:醋酸>碳酸>次氯酸 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 浓硫酸 | CuS | KMnO4 | H2S具有还原性 | |
| D | 盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
