题目内容
甲同学设计了如下图所示的原电池,电解质溶液为 FeCl2,但灯泡并不亮。乙、丙、丁同学对甲同学设计的原电池分别做了改进后,发现灯泡亮了。根据上述素材,回答下列问题:

(1)乙同学换了一个电极,如果他把铁片更换,你认为可以换成____(填化学式,下同)片或____片等。
(2)丙同学把电解质溶液换了,该溶液与铁能发生反应,但发生的不是置换反应。你认为他换成了_______溶液,电极反应式为:负极________________;正极____________
(3)丁同学没有改变电极和电解质溶液,而是用一个导管不断向溶液中通入一种黄绿色气体,则FeCl2溶液与该气体反应的离子方程式为__________________。
(2)丙同学把电解质溶液换了,该溶液与铁能发生反应,但发生的不是置换反应。你认为他换成了_______溶液,电极反应式为:负极________________;正极____________
(3)丁同学没有改变电极和电解质溶液,而是用一个导管不断向溶液中通入一种黄绿色气体,则FeCl2溶液与该气体反应的离子方程式为__________________。
(1)Zn;Al
(2)铁盐[或FeCl3,Fe2(SO4)3];Fe-2e- = Fe2+ ;2Fe3++2e- = 2Fe2+
(3)2Fe2++Cl2 = 2Fe3++2Cl-
(2)铁盐[或FeCl3,Fe2(SO4)3];Fe-2e- = Fe2+ ;2Fe3++2e- = 2Fe2+
(3)2Fe2++Cl2 = 2Fe3++2Cl-

练习册系列答案
相关题目
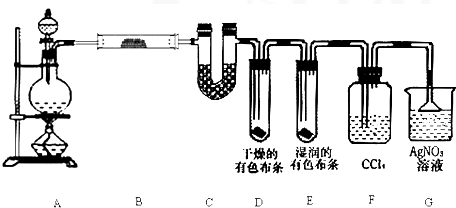
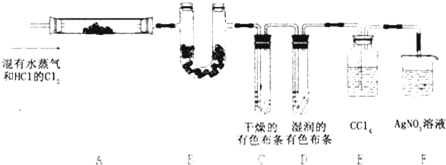
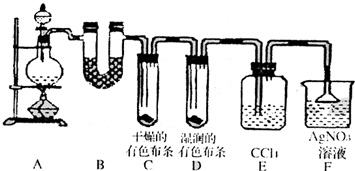 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.