题目内容
试分别用价键理论和分子轨道理论说明稀有气体不能形成双原子分子的理由。分析:从稀有气体原子间的电子不能配对成键和它们的键级为零分别加以说明。
解 稀有气体外层电子结构为ns2np6(He除外),是稳定的8电子构型,现以Ne为例加以说明。
价键理论认为:
氖的外层电子结构为2s2 2p6,所有电子都已互相成对,当两个Ne原子接近时,不能再相互配对(原子中无未成对电子),所以Ne不能形Ne2分子。
分子轨道理论认为,若能形成Ne2分子,则其分子轨道排布式为:
[KK (![]() 2s)2(
2s)2(![]()
![]() )2(
)2(![]() 2px)2(
2px)2(![]() 2py)2(
2py)2(![]() 2pz)2(
2pz)2(![]()
![]() )2(
)2(![]()
![]() )2(
)2(![]()
![]() )2]
)2]
其键级 = ![]() =
= ![]() = 0
= 0
所以Ne不能形成双原子分子。

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
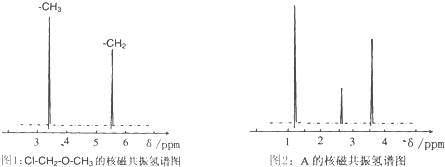
 的沸点高于
的沸点高于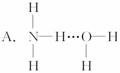

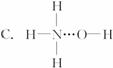

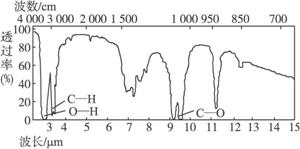
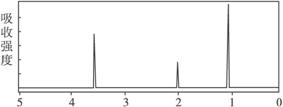
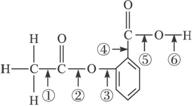
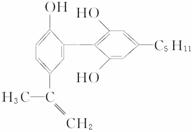
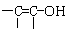 结构的物质)
。
结构的物质)
。