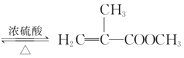��Ŀ����
����Ŀ����ʹ������к͵ζ����ⶨ���۰״�������[(g��(100 mL)-1]��
����ʵ�鲽��
��1����___(����������)��ȡ10.00mLʳ�ð״ף����ձ�����ˮϡ�ͺ�ת�Ƶ�100mL����ƿ�ж��ݣ�ҡ�ȼ��ô���״���Һ��
��2������ʽ�ζ���ȡ����״���Һ20.00mL����ƿ�У������еμ�2�η�̪��ָʾ����
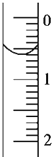
��3����ȡʢװ0.1000mol��L-1NaOH��Һ�ļ�ʽ�ζ��ܵij�ʼ���������Һ��λ����ͼ��ʾ�����ʱ�Ķ���Ϊ___mL��
��4���ζ�����___ʱ��ֹͣ�ζ�������¼ NaOH��Һ���ն������ظ��ζ�3�Ρ�
����ʵ���¼
����� | 1 | 2 | 3 | 4 |
V(��Ʒ)(mL) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(����)(mL) | 15.95 | 15.00 | 15.05 | 14.95 |
�������ݴ���������
��1����ͬѧ�ڴ�������ʱ����ã�ƽ�����ĵ�NaOH��Һ�����V��![]() mL��15.24mL����ָ������㲻����������ȷ���ݴ������ɵ����۰״���������____g����100mL��-1��
mL��15.24mL����ָ������㲻����������ȷ���ݴ������ɵ����۰״���������____g����100mL��-1��
��2���ڱ�ʵ��ĵζ������У����в�����ʹʵ����ƫ�����___��д���)��
a����ʽ�ζ����ڵζ�ʱ�ñ�NaOH��Һ��ϴ
b����ʽ�ζ��ܵļ����ڵζ�ǰ�����ݣ��ζ���������ʧ
c����ƿ�м������״���Һ���ټ�����ˮ
d����ƿ�ڵζ�ʱ����ҡ����������Һ�彦��
���𰸡���ʽ�ζ���(��10mL��Һ��) 0.60 ��Һ����ɫǡ�ñ�Ϊdz��ɫ�����ڰ�����ڲ���ɫ 4.5 b
��������
����1���״ijɷ���CH3COOH������ʽ�ζ�����ȡ��
��3������ͼƬ������
��4����̪��ָʾ�����ﵽ�ζ��յ�ʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ��
����1���ɱ��������ݿ�֪��һ���������ϴ����������������������ݽ��м��㣻
��2������c(����)= �������
�������
����1���״ijɷ���CH3COOH��Ӧ������ʽ�ζ�����ȡ��
��3���ɵζ������ݿ�֪��Һ������Ϊ0.60mL��
��4����̪��ָʾ�����ﵽ�ζ��յ�ʱ����Һ����ɫǡ�ñ�Ϊdz��ɫ�����ڰ�����ڲ���ɫ��
����1���ɱ��������ݿ�֪��һ���������ϴ�����������NaOH��Һ��ƽ�����V��![]() mL��15.00mL����10mL�״���Ʒ�к���CH3COOH x g����CH3COOH��NaOH��֪x=
mL��15.00mL����10mL�״���Ʒ�к���CH3COOH x g����CH3COOH��NaOH��֪x=![]() =0.45g�����100mL����Ʒ�к��д��������Ϊ0.45g��
=0.45g�����100mL����Ʒ�к��д��������Ϊ0.45g��![]() =4.5g�������۰״���������4.5g��(100mL)-1��
=4.5g�������۰״���������4.5g��(100mL)-1��
��2��a.��ʽ�ζ����ڵζ�ʱ�ñ�NaOH��Һ��ϴ������������ȷ����Ӱ��ζ������a�����
b. ��ʽ�ζ��ܵļ����ڵζ�ǰ�����ݣ��ζ���������ʧ��ʹV(��)ƫ������ҺŨ��ƫ�ߣ�b����ȷ��
c. ��ƿ�м������״���Һ���ټ�����ˮ����V(��)��Ӱ�죬��ҺŨ�Ȳ��䣬c�����
d. ��ƿ�ڵζ�ʱ����ҡ����������Һ�彦��������Һ�����ʵ���ƫС������V(��)ƫС����ҺŨ��ƫ�ͣ�d�����
��ѡb��