题目内容
某溶液中含有大量Fe2+、Fe3+、Mg2+和NHA.Cl- B.NO![]() C.SCN-
D.CO
C.SCN-
D.CO![]()
答案:A
提示:
提示:
| 溶液中含有Fe2+、Fe3+、Mg2+和NH4+,其c(H+)=10-2 mol·L-1说明溶液是酸性溶液,其中没有与Cl-反应生成沉淀物的离子,Cl-可以在该溶液中大量共存。答案为A。
B溶液中有Fe2+、有H+,即发生反应:3Fe2++4H++NO
|

练习册系列答案
相关题目
 人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.
人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.Ⅰ.废液组成:
| 金属元素 | Ni | Mn | Co | Fe | Cu | Zn |
| 浓度(g?L-1) | 45 | 15 | 7.5 | ≤0.1 | ≤0.05 | ≤0.05 |
步骤1:调节pH:向强酸性溶液中加入NaOH溶液调节pH到2.
此步骤中工业上不直接使用饱和Na2CO3溶液来调节溶液的pH的原因可能是
步骤2:除去Mn2+、Co2+离子:在搅拌下加入适量饱和Na2CO3溶液和NaClO溶液并控制pH≤3.5,过滤.
①Mn2+反应生成MnO2同时放出CO2,写出此反应的离子方程式:
②Co2+反应生成Co(OH)3沉淀同时放出CO2,写出此反应的离子方程式:
Ni2+可反应生成Ni(OH)3沉淀,Co2+可使Ni(OH)3转化为Co(OH)3沉淀,写出Ni(OH)3转化为Co(OH)3的离子方程式:
③此步骤中必须控制好NaClO溶液的用量,其原因可能是
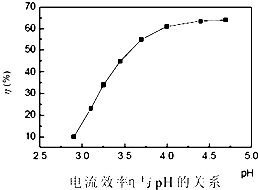
步骤3:回收镍以铅片为阳极,镍铬钛不锈钢片为阴极,电解步骤2中所得滤液,在阴极得到镍粉.电解过程中电流效率与pH的关系如图,分析图表,回答下列问题:
①pH较低时,电流效率低的原因可能是:
②电解的最佳pH范围是:
A.3.0~3.5 B.3.5~4.0 C.4.0~4.5 D.4.5~5.0.