题目内容
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是 。
(3)Y 与Z 可形成YZ42-
① YZ42-的空间构型为 (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式: 。
 (4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
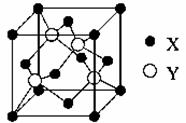
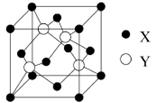
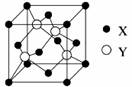
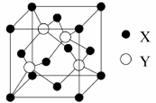
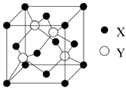
(5)X与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,X离子的数目为 。
②该化合物的化学式为 。
③已知该化合物晶体的晶胞边长为a cm,阿伏伽德罗常数为NA mol-1,则该晶体密度为____________________________g·cm-3(列出表达式即可)。
(1)sp3 (2)水分子与乙醇分子之间形成氢键
(3)①正四面体 ②CCl4或SiCl4等 (4)16NA (2分)
(5)①4 ②ZnS ③ 388/(a3·NA)(2分)(其余每空1分)

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案
相关题目
 (2013?江苏)A.[物质结构与性质]
(2013?江苏)A.[物质结构与性质]