ÌâÄ¿ÄÚÈÝ
¡¾ÌâÄ¿¡¿¡¾»¯Ñ§¡ª¡ªÑ¡ÐÞ3£ºÎïÖʽṹÓëÐÔÖÊ¡¿
I£®2015Äê¹ú²úC919´óÐÍ¿Í»úÕýʽÏÂÏߣ¬±êÖ¾×ÅÎÒ¹ú³ÉΪÊÀ½çÉÏÉÙÊý¼¸¸ö¾ßÓÐ×ÔÐÐÑÐÖÆ´óÐÍ·É»úµÄ¹ú¼ÒÖ®Ò»£¬±êÖ¾×ÅÎÒ¹úº½¿Õ¹¤Òµ½øÈëÁËеķ¢Õ¹½×¶Î¡£
£¨1£©·É»úµÄÍâ¿Çͨ³£²ÉÓÃþ£ÂÁºÏ½ð²ÄÁÏ£¬ÂÁµÄ¼Ûµç×ÓÅŲ¼Í¼Îª £¬µÚÒ»µçÀëÄÜ£ºÃ¾ £¨Ìî¡°´óÓÚ¡±»ò¡°Ð¡ÓÚ¡±£©ÂÁ¡£
£¨2£©ÏÖ´ú·É»úΪÁ˼õÇáÖÊÁ¿¶ø²»¼õÇáÍâ¿Ç³ÐѹÄÜÁ¦£¬Í¨³£²ÉÓø´ºÏ²ÄÁÏ--²£Á§ÏËάÔöÇ¿ËÜÁÏ£¬Æä³É·Ö֮һΪ»·ÑõÊ÷Ö¬£¬³£¼ûµÄE51ÐÍ»·ÑõÊ÷Ö¬Öв¿·Ö½á¹¹ÈçÏÂͼËùʾ£º
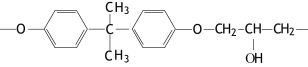

ÆäÖÐ̼Ô×ÓµÄÔÓ»¯·½Ê½Îª £¬¸öÊý±ÈΪ ¡£
II£®´óÐÍ·É»úµÄ·¢¶¯»ú±»ÓþΪº½¿Õ¹¤Òµ»Ê¹ÚÉϵġ°±¦Ê¯¡±¡£ÖÆÔì¹ý³ÌÖÐͨ³£²ÉÓÃ̼»¯ÎÙ×ö¹Ø¼ü²¿Î»µÄ²ÄÁÏ¡£
£¨3£©ÎÙÔªËØλÓÚÖÜÆÚ±íµÄµÚÁùÖÜÆÚµÚVIB×壬Çëд³öÆäÍâΧµç×ÓÅŲ¼Ê½ £»
£¨4£©ÏÂͼΪ̼»¯ÎÙ¾§ÌåµÄÒ»²¿·Ö½á¹¹£¬ ̼Ô×ÓǶÈë½ðÊôÎٵľ§¸ñµÄ¼ä϶£¬²¢²»ÆÆ»µÔÓнðÊôµÄ¾§¸ñ£¬ÐγÉÌî϶+¹ÌÈÜÌ壬Ҳ³ÆΪÌî϶»¯ºÏÎï¡£Ôڴ˽ṹÖУ¬ÆäÖÐÎÙÔ×ÓÓÐ ¸ö£¬1¸öÎÙÔ×ÓÖÜΧ¾àÀëÎÙÔ×Ó×î½üµÄ̼Ô×ÓÓÐ ¸ö £¬ÏÂÁнðÊôÔªËصĶѻý·½Ê½Óë̼»¯ÎÙ¾§°ûÖÐ̼Ô×ÓºÍÎÙÔ×ÓËù´¦Î»ÖÃÀàËƵÄÊÇ ¡£
A. Fe Cu B.Ti Au C.Mg Zn D.Cu Ag
£¨5£©¼ÙÉè¸Ã²¿·Ö¾§ÌåµÄÌå»ýΪVcm3£¬Ì¼»¯ÎÙµÄĦ¶ûÖÊÁ¿ÎªM g/mol£¬ÃܶÈΪb g/cm3,Ôò°¢·ü¼ÓµÂÂÞ³£ÊýNAÓÃÉÏÊöÊý¾Ý¿ÉÒÔ±íʾΪ ¡£
¡¾´ð°¸¡¿£¨1£© £¨1·Ö£©£¬´óÓÚ£¨1·Ö£©
£¨1·Ö£©£¬´óÓÚ£¨1·Ö£©
£¨2£©sp2£¨1·Ö£©sp3£¨1·Ö£©,2£º1
£¨3£©5d46s2»òÕß5d56s1£¨2·Ö£©
£¨4£©6£¨1·Ö£©£¬6£¨1·Ö£©£¬C£¨2·Ö£©£¨5£©![]() £¨3·Ö£©
£¨3·Ö£©
¡¾½âÎö¡¿
ÊÔÌâ·ÖÎö£º£¨1£©ÂÁÊÇ13ºÅÔªËØ£¬×îÍâ²ãÓÐ3¸öµç×Ó£¬¸ù¾ÝºËÍâµç×ÓÅŲ¼¹æÂÉ£¬ÂÁµÄ¼Ûµç×ÓÅŲ¼Í¼Îª £»Ã¾¡¢ÂÁÊôÓÚͬһÖÜÆÚÔªËØ£¬Ã¾Ô×ÓµÄ×îÍâ²ãµç×ÓÅŲ¼Îª2s2£¬´¦ÓÚÈ«³äÂú״̬£¬Ïà¶Ô±È½ÏÎȶ¨£¬µÚÒ»µçÀëÄܱÈͬÖÜÆÚÏàÁÚÔªËصĵÚÒ»µçÀëÄܶ¼´ó£¬ËùÒÔµÚÒ»µçÀëÄÜ£ºÃ¾´óÓÚÂÁ£»
£»Ã¾¡¢ÂÁÊôÓÚͬһÖÜÆÚÔªËØ£¬Ã¾Ô×ÓµÄ×îÍâ²ãµç×ÓÅŲ¼Îª2s2£¬´¦ÓÚÈ«³äÂú״̬£¬Ïà¶Ô±È½ÏÎȶ¨£¬µÚÒ»µçÀëÄܱÈͬÖÜÆÚÏàÁÚÔªËصĵÚÒ»µçÀëÄܶ¼´ó£¬ËùÒÔµÚÒ»µçÀëÄÜ£ºÃ¾´óÓÚÂÁ£»
£¨2£©¸ù¾Ý»·ÑõÊ÷Ö¬µÄ½á¹¹¼òʽ¿ÉÖª£¬·Ö×ÓÖÐ̼ԪËز¿·ÖÐγɵ¥¼ü£¬²¿·ÖÐγɱ½»·£¬Òò´Ë̼Ô×ÓµÄÔÓ»¯¹ìµÀÀàÐÍÊÇsp2¡¢sp3£»¶ÔÓ¦¸öÊý±ÈΪ12£º6£½2£º1¡£
£¨3£©ÎÙÔªËØλÓÚÖÜÆÚ±íµÄµÚÁùÖÜÆÚµÚVIB×壬ÆäÍâΧµç×ÓÅŲ¼Ê½Îª5d56s1¡£
£¨4£©Ì¼»¯ÎÙ¾§Ìå½á¹¹ÀàËÆÓÚ½ðÊôZn¡¢Ti¡¢MgµÄÁù·½×îÃܶѻý£¬²î±ðÔÚÓÚÿ²ãÊÇ̼ºÍÎÙ½»ÌæÅÅÁеģ¬ËùÒÔÅäλÊý¼õ°ëΪ6¸ö£¬¼´Ôڴ˽ṹÖУ¬ÆäÖÐÎÙÔ×ÓÓÐ6¸ö£¬1¸öÎÙÔ×ÓÖÜΧ¾àÀëÎÙÔ×Ó×î½üµÄ̼Ô×ÓÓÐ6¸ö£¬ÏÂÁнðÊôÔªËصĶѻý·½Ê½Óë̼»¯ÎÙ¾§°ûÖÐ̼Ô×ÓºÍÎÙÔ×ÓËù´¦Î»ÖÃÀàËƵÄÊÇC¡£
£¨5£©ÀûÓþù̯·¨¼ÆË㣬¸Ã¾§°ûÖÐÎÙÔ×Ó¸öÊý£½2¡Á6¡Á1/3¡Á1/2+2¡Á1/2+1+6¡Á1/3£½6¸ö£¬¾§°ûÖÐ̼Ô×Ó¸÷Ϊ6¸ö¡£ÒѾ֪µÀ¾§°ûÌå»ý£¬¸ù¾ÝÃܶȣ½m¡ÂV£¬b£½6M¡Â(NA¡ÁV),ËùÒÔNA£½![]() ¡£
¡£
¡¾ÃûʦµãÇç¡¿¿¼²é¹ìµÀÅŲ¼Í¼¡¢µÚÒ»µçÀëÄÜ¡¢ÔÓ»¯ÀàÐ͵ÄÅжϣ¬¾§°ûµÄ¼ÆËãµÈ֪ʶ¡£

 Ò»ÏßÃûʦȨÍþ×÷Òµ±¾ÏµÁдð°¸
Ò»ÏßÃûʦȨÍþ×÷Òµ±¾ÏµÁд𰸡¾ÌâÄ¿¡¿Ì¼¼°Æ仯ºÏÎïÔÚÄÜÔ´¡¢²ÄÁϵȷ½Ãæ¾ßÓй㷺µÄÓÃ;¡£»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©Ì¼ËáºÍ²ÝËá¾ùΪ¶þÔªÈõËᣬÆäµçÀë·ÖΪÁ½²½½øÐУ¬ÒÑÖªÆäµçÀë³£ÊýµÄÓйØÊý¾ÝÈçÏÂ±í£ºÏòNa2CO3ÈÜÒºÖеμӲÝËáÈÜÒº£¬¿ªÊ¼Ê±Ëù·¢Éú·´Ó¦µÄÀë×Ó·½³ÌʽΪ ¡£
H2CO3 | H2C2O4 | |
K1 | 4.2¡Á10-7 | 5.4¡Á10-2 |
K2 | 5.6¡Á10-11 | 5.4¡Á10-5 |
£¨2£©³£ÎÂʱ£¬CºÍCOµÄȼÉÕÈÈ¡÷H·Ö±ðΪ£394.0 kJ¡¤mol-1¡¢£283.0 kJ¡¤mol-1£¬¸ÃÌõ¼þÏÂCת»¯ÎªCOµÄÈÈ»¯Ñ§·½³ÌʽΪ ¡£
£¨3£©ÇâÆøºÍÒ»Ñõ»¯Ì¼ÔÚÒ»¶¨Ìõ¼þÏ¿ɺϳɼ״¼£¬·´Ó¦ÈçÏÂ
2H2(g£©£«CO(g£©![]() CH3OH(g£© ¡÷H£½Q kJ¡¤mol-1¡£
CH3OH(g£© ¡÷H£½Q kJ¡¤mol-1¡£
¢Ù¸Ã·´Ó¦ÔÚ²»Í¬Î¶ÈϵĻ¯Ñ§Æ½ºâ³£Êý(K£©ÈçÏÂ±í£º
ζÈ(¡æ£© | 250 | 300 | 350 |
K(L2¡¤mol-1£© | 2.041 | 0.270 | 0.012 |
ÓÉ´Ë¿ÉÅжÏQ 0(Ìî¡°£¾¡±¡¢¡°£½¡±»ò¡°£¼¡±£©
¢ÚÒ»¶¨Î¶ÈÏ£¬½«6 mol H2ºÍ2mol CO³äÈëµ½Ìå»ýΪ2 LµÄÃܱÕÈÝÆ÷ÖУ¬10 minʱ·´Ó¦´ïµ½Æ½ºâ״̬£¬´Ëʱ²âµÃc(CO£©£½0.2 mol¡¤L-1£¬¸ÃζÈϵÄƽºâ³£ÊýK£½ ¡£0¡«10 minÄÚ£¬·´Ó¦ËÙÂÊv(CH3OH£©£½ ¡£
¢ÛÔÚÁ½¸öÃܱÕÈÝÆ÷Öзֱ𶼳äÈë20 mol H2ºÍ10 mol CO£¬²âµÃÒ»Ñõ»¯Ì¼µÄƽºâת»¯ÂÊËæζÈ(T£©¡¢Ñ¹Ç¿(p£©µÄ±ä»¯ÈçÏÂͼËùʾ£º
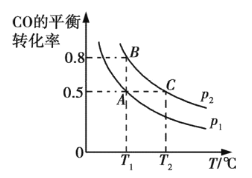
A¡¢BÁ½µãѹǿ´óС¹Øϵ£ºp1 p2(Ìî¡°£¾¡±¡¢¡°£½¡±»ò¡°£¼¡±£©¡£ÈôAµã¶ÔÓ¦ÈÝÆ÷µÄÈÝ»ýΪ20 L£¬ÔòBµã¶ÔÓ¦µÄÈÝÆ÷µÄÈÝ»ýΪ L¡£