��Ŀ����
�����и��仯�У�EΪ��������ɫ��ζ��Һ�壬FΪ����ɫ��ĩ��GΪ��������ɫ���壨��Ӧ��������ʡ�ԣ���
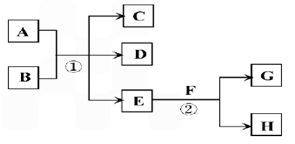
�ش��������⣺
��1��д��H�ĵ���ʽ��_______________��
��2������Ӧ���ڼ��������½��У�AΪ���ʣ�CΪ��ɫ�д̼�����ζ�����壬DΪ��ɫ��ζ�����壬��C��D�����������ʹ�����ʯ��ˮ����ǣ���Ӧ�ٵĻ�ѧ����ʽ�� ___________��
��ʵ����Ҫ�����C��D��E�����������������������Ⱥ�˳���� ___________���û�ѧʽ��գ����ڼ���D����ǰ�����ȥC���壬�����Լ���_____________ ����Ӧ�����ӷ���ʽ��_____________ ��
����֪��A(s)+O2(g) =AO2(g) ��H����393.5kJ��mol-1�� 2A(s)+O2(g) =2AO(g) ��H����221.0kJ��mol-1����AO��ȼ���ȵ��Ȼ�ѧ����ʽ_________________________��
��AO2����Ȼ��ѭ��ʱ����̼��Ʒ�Ӧ��̼�����һ���������ʣ�����Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ___________��
��3������Ӧ������Һ�н��У�A��һ�ֳ���һԪǿ�B��һ����ʽ�Σ�D��һ�����壬��B�����������ʹƷ����Һ��ɫ�����壬�ڼ��������£���A����ʱ����Ӧ�ٵ����ӷ���ʽ��_______________ ��
��4������Ӧ������Һ�н��У�A��һ��ǿ�ᣬB��һ�ֺ������ֽ���Ԫ�ص��Σ���B��ˮ��Һ�Լ��ԣ�A��B���ɶ�����Ԫ����ɣ���A����ʱ��C��D��������ˮ����A����ʱ��Ӧ�ٵ����ӷ���ʽ��_________________ ��
��1��д��H�ĵ���ʽ��_______________��
��2������Ӧ���ڼ��������½��У�AΪ���ʣ�CΪ��ɫ�д̼�����ζ�����壬DΪ��ɫ��ζ�����壬��C��D�����������ʹ�����ʯ��ˮ����ǣ���Ӧ�ٵĻ�ѧ����ʽ�� ___________��
��ʵ����Ҫ�����C��D��E�����������������������Ⱥ�˳���� ___________���û�ѧʽ��գ����ڼ���D����ǰ�����ȥC���壬�����Լ���_____________ ����Ӧ�����ӷ���ʽ��_____________ ��
����֪��A(s)+O2(g) =AO2(g) ��H����393.5kJ��mol-1�� 2A(s)+O2(g) =2AO(g) ��H����221.0kJ��mol-1����AO��ȼ���ȵ��Ȼ�ѧ����ʽ_________________________��
��AO2����Ȼ��ѭ��ʱ����̼��Ʒ�Ӧ��̼�����һ���������ʣ�����Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ2��10-4mol/L�������ɳ�������CaCl2��Һ����СŨ��Ϊ___________��
��3������Ӧ������Һ�н��У�A��һ�ֳ���һԪǿ�B��һ����ʽ�Σ�D��һ�����壬��B�����������ʹƷ����Һ��ɫ�����壬�ڼ��������£���A����ʱ����Ӧ�ٵ����ӷ���ʽ��_______________ ��
��4������Ӧ������Һ�н��У�A��һ��ǿ�ᣬB��һ�ֺ������ֽ���Ԫ�ص��Σ���B��ˮ��Һ�Լ��ԣ�A��B���ɶ�����Ԫ����ɣ���A����ʱ��C��D��������ˮ����A����ʱ��Ӧ�ٵ����ӷ���ʽ��_________________ ��
��1��NaOH
��2��C��2H2SO4��Ũ����CO2����2SO2����2H2O
��H2O��SO2��CO2������KMnO4��Һ��2MnO4-+5SO2+H2O=2Mn2++5SO42-+4H+
��CO��g��+ 1/2 O2��g��=CO2(g)����H=-283.0kJ��mol-1
��5.6��10-5mol/L��
��3��2OH����NH4+��HSO3-��NH3����2H2O��SO32-
��4��4H����AlO2-��Al3����2H2O
��2��C��2H2SO4��Ũ����CO2����2SO2����2H2O
��H2O��SO2��CO2������KMnO4��Һ��2MnO4-+5SO2+H2O=2Mn2++5SO42-+4H+
��CO��g��+ 1/2 O2��g��=CO2(g)����H=-283.0kJ��mol-1
��5.6��10-5mol/L��
��3��2OH����NH4+��HSO3-��NH3����2H2O��SO32-
��4��4H����AlO2-��Al3����2H2O

��ϰ��ϵ�д�
 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�
�����Ŀ




 Ti
Ti
 Ti
Ti