��Ŀ����
18������A��B��C��D��E����������֪��1mol�������ֱ���ȫȼ�գ�������134.4L CO2����״����������C��ȫȼ��ʱ�����ɵ�ˮ�����ʵ�����CO2�ࣻ
��A��D����ʹ��ˮ��ɫ������1mol D���Ժ�1mol H2��Ӧ����1mol A��1mol A�ֿɼ�����1mol H2��Ӧ������1mol C��
��C������ˮ������KMnO4��Һ��Ӧ��
��A���ڶ���ͬ���칹�壬����Cֻ����һ��A��������Ӧ���ã�
��B����м�����¿��Ը�Һ�巴Ӧ����������ˮ�����Ը��������Һ��Ӧ��
��B�ܺ�������ַ�Ӧ����E��
��ش��������⣺
��1��д�������������Aϩ����B��������C������
��2����C��һ±��������3��ͬ���칹�壮
��3���á�ϵͳ����������D������3��3-����-1-��Ȳ��
��4�����ϼ�����������Ϊ��ˮ�������ȡ�����У�BCE���á�A��B��C�������𣩣�
��5��д����������������A��HCl�ڴ��������µļӳɷ�Ӧ����ʽ��CH2=CHC��CH3��3+HCl$\stackrel{����}{��}$ClCH2CH2C��CH3��3��
���� ��1 mol�������ֱ���ȫȼ�գ�������CO2Ϊ$\frac{134.4L}{22.4L/mol}$=6mol��������о�����6��Cԭ�ӣ�����C��ȫȼ��ʱ�����ɵ�ˮ�����ʵ�����CO2�࣬�����ɵ�ˮӦ����6mol���ʷ�����Hԭ����Ŀ����12������Ϊ����ʱHԭ����Ŀ���Ϊ14������C�ķ���ʽΪC6H14�����Ϣ���C������ˮ������KMnO4��Һ��Ӧ��
��A��D����ʹ��ˮ��ɫ������̼̼�����ͼ�������1 mol D���Ժ�1 mol H2��Ӧ����1 mol A��1 mol A�ֿɼ�����1 mol H2��Ӧ����1 mol��C����D�к���2��̼̼˫������1��̼̼������A�к���1��̼̼˫������D�ķ���ʽΪC6H10��A�ķ���ʽΪ��C6H12��
��A���ڶ���ͬ���칹�壬����Cֻ����һ��A��������Ӧ���ã���CΪCH3CH2C��CH3��3����AΪCH2=CHC��CH3��3����DΪCH��CC��CH3��3��
��B����м�����¿�����Һ�巴Ӧ����������ˮ�����Ը��������Һ��Ӧ����BΪ���� ����
����
��B����������ַ�Ӧ����EΪ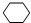 ��
��
��� �⣺��1 mol�������ֱ���ȫȼ�գ�������CO2Ϊ$\frac{134.4L}{22.4L/mol}$=6mol��������о�����6��Cԭ�ӣ�����C��ȫȼ��ʱ�����ɵ�ˮ�����ʵ�����CO2�࣬�����ɵ�ˮӦ����6mol���ʷ�����Hԭ����Ŀ����12������Ϊ����ʱHԭ����Ŀ���Ϊ14������C�ķ���ʽΪC6H14�����Ϣ���C������ˮ������KMnO4��Һ��Ӧ��
��A��D����ʹ��ˮ��ɫ������̼̼�����ͼ�������1 mol D���Ժ�1 mol H2��Ӧ����1 mol A��1 mol A�ֿɼ�����1 mol H2��Ӧ����1 mol��C����D�к���2��̼̼˫������1��̼̼������A�к���1��̼̼˫������D�ķ���ʽΪC6H10��A�ķ���ʽΪ��C6H12��
��A���ڶ���ͬ���칹�壬����Cֻ����һ��A��������Ӧ���ã���CΪCH3CH2C��CH3��3����AΪCH2=CHC��CH3��3����DΪCH��CC��CH3��3��
��B����м�����¿�����Һ�巴Ӧ����������ˮ�����Ը��������Һ��Ӧ����BΪ���� ����
����
��B����������ַ�Ӧ����EΪ ��
��
��1��������������֪��A����ϩ����B���ڷ�������C����������
�ʴ�Ϊ��ϩ������������������
��2��CΪCH3CH2C��CH3��3�������к���3��Hԭ�ӣ�����C��һ±��������3��ͬ���칹�壬
�ʴ�Ϊ��3��
��3��DΪCH��CC��CH3��3������Ϊ��3��3-����-1-��Ȳ��
�ʴ�Ϊ��3��3-����-1-��Ȳ��
��4��ϩ����Ȳ�������巢���ӳɷ�Ӧ��������������Ϊ��ˮ�������ȡ�����У�������������������
�ʴ�Ϊ��BCE��
��5����������������A��HCl�ڴ��������µļӳɷ�Ӧ����ʽ��CH2=CHC��CH3��3+HCl$\stackrel{����}{��}$ClCH2CH2C��CH3��3��
�ʴ�Ϊ��CH2=CHC��CH3��3+HCl$\stackrel{����}{��}$ClCH2CH2C��CH3��3��
���� ���⿼���л�����ƶϣ�������������Ŀ���ؼ��Ǹ���ȼ�����ɶ�����̼��ˮ����ȷ��C�ķ���ʽ���ٽ�Ϸ����ķ�Ӧ�ƶϣ����ؿ���ѧ���ķ�������������

 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�| A�� | ��ɫ��Һ�У�Al3+��Cl-��MnO4-��SO42- | |
| B�� | ���д���Fe3+����Һ�У�Na+��Mg2+��NO3-��SCN- | |
| C�� | ���������ܲ�����������Һ�У�CH3COO-��NH4+��SO42-��I- | |
| D�� | ʹ��̪���ɫ����Һ��CO32-��Cl-��F-��K+ |
����Ҫ���������ữKMnO4��Һ����ɫ����ʱ��tA��tB�����������=����������
��д���÷�Ӧ�����ӷ���ʽ5H2C2O4+2MnO4-+6H+=10CO2��+2Mn2++8H2O��
��2��ʵ������ƿ������ɳ���Ҷ�����Ʒ��С�����������Ӧ��ԭ�����ⶨ�京��������Ϊ��
������250mL��Һ��ȷ����5.0g�Ҷ�����Ʒ�����250mL��Һ��
�ڵζ���ȷ��ȡ25.00mL������Һ����ƿ�У����������ữ����0.1000mol•L-1KMnO4��Һװ����ʽ�����ʽ����ʽ�����ζ��ܣ����еζ���������ʵ���з��֣��յ�������KMnO4��Һʱ����ҺѸ�ٱ���Ϻ�ɫ������ƿҡ��һʱ����Ϻ�ɫ������ʧ���ټ����μ�ʱ���Ϻ�ɫ�ͺܿ���ɫ�ˣ������ԭ��Ӧ�����ɵ������Ӿ��д����ã����������ɫ��ӿ죮�����������һ�θ��������Һ����ƿ�ڵ���ɫǡ�ñ���Ϻ�ɫ�Ұ���Ӳ��仯��֤���ﵽ�ζ��յ㣮
�ۼ��㣺���ظ���������2�Σ���¼ʵ���������£�
| ��� | �ζ�ǰ������mL�� | �ζ��������mL�� |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 22.10 |
�������������в����ᵼ�²ⶨ���ƫ�ߵ���ACD��
A δ�ñ�Ũ�ȵ�����KMnO4��Һ��ϴ�ζ���
B �ζ�ǰ��ƿ������ˮ
C �ζ�ǰ�ζ��ܼ��첿�������ݣ��ζ���������ʧ
D��С�Ľ���������KMnO4��Һ������ƿ��
E���۲����ʱ���ζ�ǰ���ӣ��ζ����ӣ�
| A�� | KOH��NH4Cl | B�� | SO2��SiO2 | C�� | MgO��Na2O2 | D�� | CCl4��KCl |
| A�� | 60g�������辧���У������ۼ�NA�� | |
| B�� | ���³�ѹ�£�22.4L H2�к�������Ϊ2NA�� | |
| C�� | ��0.5mol�����Ƶ���Һ����������Ϊ3NA�� | |
| D�� | 0.5molþ��������������ȫ��Ӧ����ʧȥNA������ |
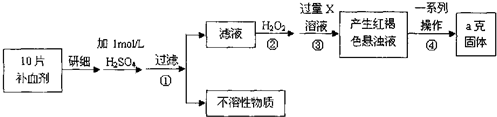
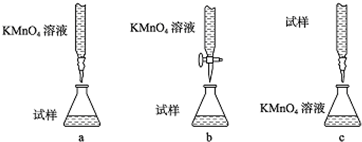
 ����֪�Ҵ��ļ���ʽΪ
����֪�Ҵ��ļ���ʽΪ ��
��
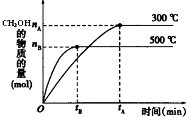 һ�������£������Ϊ3L���ܱ������з�ӦCO��g��+2H2��g��?CH3OH��g���ﵽ��ѧƽ��״̬��
һ�������£������Ϊ3L���ܱ������з�ӦCO��g��+2H2��g��?CH3OH��g���ﵽ��ѧƽ��״̬��
 ��
��