题目内容
7.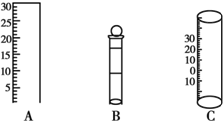 如图所示为中学化学实验中几种常见仪器的部分结构:
如图所示为中学化学实验中几种常见仪器的部分结构:(1)请写出上述仪器的名称:A量筒;B容量瓶;C温度计.
(2)若要配制一定物质的量浓度的硫酸溶液,必须使用上述仪器中的AB(填字母).
(3)上述仪器在使用之前必须检查是否漏水的是B(填字母),检查该仪器是否漏水的具体操作方法是往瓶内加水,塞好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立过来,观察瓶塞周围是否漏水;如不漏水,把瓶塞旋转180°塞紧,仍把瓶倒立过来,再检验是否漏水.两次均不漏水才表明容量瓶不漏水.
分析 (1)根据常见计量仪器的结构特征分析;
(2)根据配制一定物质的量浓度的溶液的配制步骤选择使用的仪器,注意硫酸为液体,需要使用量筒量取;
(3)带有活塞或瓶塞的装置使用前要检查是否漏水.
解答 解:(1)A无0刻度,从下到上刻度逐渐增大,应为量筒,B有活塞,且只有一个刻度线,应为容量瓶,C刻度有负值,应为温度计,故答案为:量筒;容量瓶;温度计;
(2)用98%的浓H2SO4配制一定物质的量浓度的硫酸溶液的操作步骤有:计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,
所以需要的仪器有:量筒、容量瓶、烧杯、玻璃棒、胶头滴管等,故答案为:AB;
(3)容量瓶使用前需要检验是否漏水,往瓶内加水,塞好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立过来,观察瓶塞周围是否漏水;如不漏水,把瓶塞旋转180°塞紧,仍把瓶倒立过来,
故答案为:B;往瓶内加水,塞好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立过来,观察瓶塞周围是否漏水;如不漏水,把瓶塞旋转180°塞紧,仍把瓶倒立过来,再检验是否漏水.两次均不漏水才表明容量瓶不漏水.
点评 本题考查常见计量仪器的使用,题目难度不大,注意常见计量仪器的结构特征和使用方法.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
17.三草酸合铁酸钾晶体K3[Fe(C2O4)3]?3H2O可用于摄影和蓝色印刷.某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究.请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程.
限选试剂:浓硫酸、1.0mol•L-1HNO3、1.0mol•L-1盐酸、1.0mol•L-1NaOH、3%H2O2、0.1mol•L-1 KI、0.1mol•L-1CuSO4、20%KSCN、澄清石灰水、氧化铜、蒸馏水.
(1)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3.通过利用焰色反应可验证固体产物中是否含有钾元素.
(2)固体产物中铁元素存在形式的探究.
①提出合理假设
假设1:全部是铁单质;
假设2:全部为FeO;
假设3:同时存在铁单质和FeO.
②设计实验方案证明你的假设
③实验过程
根据②中方案进行实验.在写出实验步骤、预期现象与结论.
限选试剂:浓硫酸、1.0mol•L-1HNO3、1.0mol•L-1盐酸、1.0mol•L-1NaOH、3%H2O2、0.1mol•L-1 KI、0.1mol•L-1CuSO4、20%KSCN、澄清石灰水、氧化铜、蒸馏水.
(1)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3.通过利用焰色反应可验证固体产物中是否含有钾元素.
(2)固体产物中铁元素存在形式的探究.
①提出合理假设
假设1:全部是铁单质;
假设2:全部为FeO;
假设3:同时存在铁单质和FeO.
②设计实验方案证明你的假设
③实验过程
根据②中方案进行实验.在写出实验步骤、预期现象与结论.
| 实验步骤 | 预期现象与结论 |
| 步骤1:取适量固体产物与试管中,加入足量蒸馏水,充分振荡使碳酸钾完全溶解.分离不溶固体与溶液,用蒸馏水充分洗涤不溶固体 | 部分固体不溶解 |
| 步骤2:向试管中加入适量硫酸铜溶液,再加入少量不溶固体,充分振荡 | (1)若蓝色溶液颜色及加入的不溶固体无明显变化,则假设2成立. (2)若蓝色溶液颜色明显改变,且有暗红色固体生成,则证明有铁单质存在 |
| 步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤至洗涤液无色,取少量固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN | 结合步骤2中的(2): (1)若溶液基本无色,则假设1成立 (2)若溶液呈血红色,则假设3成立 |
16.向下列溶液滴加稀盐酸,生成白色沉淀,继续滴加稀盐酸,沉淀又溶解的是( )
| A. | Na2SiO3 | B. | BaCl2 | C. | AgNO3 | D. | NaAlO2 |
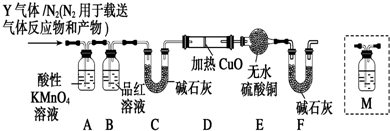
3. 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y 同时通入盛有足量氯化钡溶液的洗气瓶中(如图所示),下列有关说法正确的是( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | B. | 在Z导管出来的气体中无二氧化碳 | ||
| C. | 洗气瓶中产生的沉淀是硫酸钡 | D. | 在Z导管口有红棕色气体出现 |


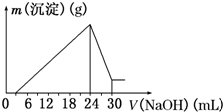 铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程:
铝是现今人类生产生活中使用广泛性仅次于铁的重要金属.工业上常以“钒土矿”为原料来冶炼金属铝.已知:钒土的主要成分是Al2O3(其中含有Fe2O3、SiO2等杂质).为了检测某“钒土矿”样中Al2O3的含量,进行了如下实验过程: .
.