题目内容
14.在一定条件下,将3molA和1molB两种其他混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)═xC(g)+2D(s).2min 时该反应达到平衡,生成了0.8molD,并测得C的浓度为0.2mol•L-1.下列判断错误的是( )| A. | x=1 | |
| B. | 充入稀有气体增大体系压强,可提高该反应的反应速率 | |
| C. | 平衡时A与B的转化率相等,均为40% | |
| D. | 平衡时B与C的浓度之比为3:2 |
分析 依据化学平衡的三段式计算进行分析,结合题中各量列式计算以及根据浓度对反应速率的影响判断;
A、利用物质的量之比等于化学计量数之比计算x的值;
B、固定容积充入稀有气体增大体系压强,各物质的浓度不变,据此判断;
C、利用转化率定义计算;
D、根据平衡浓度求出比值;
解答 解:平衡时C的浓度为0.2mol•L-1,C的物质的量为0.2mol•L-1×2L=0.4mol,
3A(g)+B(g)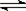 xC(g)+2D(g)
xC(g)+2D(g)
起始量(mol) 3 1 0 0
变化量(mol) 1.2 0.4 0.4 0.8
平衡量(mol) 1.8 0.6 0.4 0.8
依据上式分析计算:
A、物质的量之比等于化学计量数之比,故0.4mol:0.8mol=x:2,解得x=1,故A正确;
B、固定容积充入稀有气体增大体系压强,各物质的浓度不变,所以反应速率不变,故B错误;
C、A与B的转化率分别为$\frac{1.2mol}{3mol}$=40%,$\frac{0.4mol}{1mol}$=40%,两者相等,故C正确;
D、平衡时B与C的浓度分别为$\frac{0.6mol}{2L}$=0.3mol/L,$\frac{0.4mol}{2L}$=0.2mol/L,两者浓度之比为3:2,故D正确;
故选B.
点评 本题考查化学平衡的有关计算、转化率的有关计算、平衡状态的判断等,难度中等,注意影响反应速率的因素,浓度不变,反应速率不变.

练习册系列答案
相关题目
18.2H2S+SO2═3S↓+2H2O的反应中,当有4×6.02×1023个电子发生转移时,得到的氧化产物比还原产物多( )
| A. | 64 g | B. | 32 g | C. | 1.5mol | D. | 3 mol |
19.下列说法正确的是( )
| A. | 对于二元酸H2X,若NaHX溶液呈酸性,则H2X为强酸 | |
| B. | 升高温度,Na2A溶液的pH增大,H2A为弱酸 | |
| C. | 向烧碱溶液中通人CO2,一定存在c(Na+)=c(CO32-)+c(HCO3-)+c(H2C03) | |
| D. | 常温下,稀释氢氟酸溶液,$\frac{c({F}^{-})}{c(HF)•c(O{H}^{-})}$增大 |
2.在密闭容器中发生反应X(g)+2Y(g)?2Z(g),若开始时,只加入X、Y两种物质,达到平衡后,测得混合气体中反应物总物质的量与生成物的物质的量相等,则X、Y的初始物质的量之比范围最准确的是( )
| A. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{3}{2}$ | B. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<$\frac{1}{2}$ | C. | $\frac{1}{4}$<$\frac{n(X)}{n(Y)}$<4 | D. | $\frac{1}{2}$<$\frac{n(X)}{n(Y)}$<4 |
19.开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
①由表中数据判断Q<0(填“>”、“<”或“=”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
Ⅰ、已知:①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(1)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:CH3OH(1)+O2(g)=CO(g)+2H2O(1)△H=-442.8kJ•mol-1.
Ⅱ、工业上采用下列反应合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H=Q kJ/mol
(1)下列一定能说明该可逆反应达到化学平衡状态的是(填字母序号)CD.
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的密度不变
C.CH3OH、CO、H2的浓度都不再发生变化 D.混合气体的平均相对分子质量不变
(2)如表所列数据是该可逆反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡测得c(CO)=0.2mol/L,此时对应的温度为250℃℃;CO的转化率为80%;
(3)一定温度下,将1mol CO和3molH2分别充入容积均为1L的甲(恒压)、乙(恒容)密闭容器中.若经过60s乙容器中反应达到平衡,则甲容器中达到平衡时所需的时间<60s(填“>”、“<”或“=”).
(4)要提高CO的转化率并且提高反应速率,可采取的措施是D(填字母).
A.升温 B.加入催化剂 C.增加CO的浓度
D.体积不变通入H2 E.体积不变通入惰性气体 F.分离出甲醇.
3.下列说法正确的是( )
| A. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| B. | 工业上利用油脂生产肥皂、用淀粉酿酒、用纤维素生产酒精 | |
| C. | 酸性高锰酸钾紫色溶液中加入植物油充分振荡后,溶液颜色不会因反应褪去 | |
| D. | 蛋白质和油脂在发生腐败变质时,均会产生含NH3的刺激性气味 |
4.下列事实不能说明元素的金属性或非金属性相对减弱的是( )
| 序号 | 事实 | 推论 |
| A | Ca(OH)2的碱性强于Mg(OH)2 | 金属性:Ca>Mg |
| B | 与冷水反应,Na比Mg剧烈 | 金属性:Na>Mg |
| C | SO2与NaHCO3溶液反应生成CO2 | 非金属性:S>C |
| D | t℃时,Br2+H2?2HBr K=5.6×107 I2+H2?2HI K=43 | 非金属性:Br>I |
| A. | A | B. | B | C. | C | D. | D |