题目内容
20.碳及其化合物有广泛的用途.(1)反应C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是BC.
A.增加碳的用量 B.升高温度 C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1
则反应 CO(g)+H2O(g)?CO2(g)+H2(g) 的△H=-41.2kJ•mol-1.
(3)在298k温度下,将CO(g)和H2O(g)各0.16mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如表数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②若反应在398K进行,某时刻测得n(CO)=0.5mol n(H2O)=1.0mol,n(CO2)=1.0mol n(H2)=1.2mol则此时V(正)<V(逆)(填“>”、“<”或“=”).
(4)CaS在一定条件下经原子利用率100%的高温反应生成CaSO4,该反应的化学方程式为CaS+2O2$\frac{\underline{\;高温\;}}{\;}$CaSO4;在一定条件下,CO2可与对二甲苯反应,在其苯环上引入一个羧基,对二甲苯的结构产简式为:
 ,产物的结构简式为
,产物的结构简式为 .
.
分析 (1)该反应是一个反应前后气体体积增大的吸热反应,升高温度、减小压强、减少生成物的量都能使平衡向正反应方向移动提高H2产率;
(2)利用盖斯定律构造目标热化学方程式,反应热也进行相应的运算;
(3)①先求出平衡时各物质的浓度,再根据平衡常数表达式为K=$\frac{c(H{\;}_{2})×c(CO{\;}_{2})}{c(CO)×c(H{\;}_{2}O)}$计算;
②计算可知此时的浓度商Q余与K比较判断;
(4)根据“CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO4”可知另一种反应物为氧气,据此写出反应的化学方程式;在对二甲苯的苯环上添上应该羧基即可得到该有机物.
解答 解:(1)提高H2产率,应改变体积平衡向正反应方向移动,
A.碳为固体,增加碳的用量,不影响平衡移动,故A错误;
B.正反应为吸热反应,升高温度,平衡向正反应方向移动,能提高H2产率,故B正确;
C.用CO吸收剂除去CO,CO的浓度降低,平衡向正反应方向移动,能提高H2产率,故C正确;
D.加入催化剂,加快反应速率,缩短到达平衡的时间,不影响平衡移动,故D错误,
故答案为:BC;
(2)已知:①C(s)+H2O(g)?CO(g)+H2(g),△H=+131.3kJ•mol-1,
②C(s)+CO2(g)?2CO(g),△H=+172.5kJ•mol-1
根据盖斯定律,①-②得:CO(g)+H2O(g)?CO2(g)+H2(g),△H=131.3kJ•mol-1-172.5kJ•mol-1=-41.2kJ•mol-1,
故答案为:-41.2;
(3)①CO和H2O反应了0.06mol,则CO2和H2生成了0.06mol,平衡时各物质的浓度为:反应物CO和H2O为0.05mol/L,生成物CO2和H2为0.03mol/L,
平衡常数表达式为K=$\frac{c(H{\;}_{2})×c(CO{\;}_{2})}{c(CO)×c(H{\;}_{2}O)}$=$\frac{0.03mol/L×0.03mol/L}{0.05mol/L×0.05mol/L}$=$\frac{9}{25}$,
故答案为:$\frac{9}{25}$;
②若反应在398K进行,某时刻测得n(CO)=0.5mol n(H2O)=1.0mol,n(CO2)=1.0mol n(H2)=1.2mol则此时浓度商Q=$\frac{c(H{\;}_{2})×c(CO{\;}_{2})}{c(CO)×c(H{\;}_{2}O)}$=$\frac{1×1.2}{0.5×1}$=$\frac{12}{5}$>K,所以平衡向逆反应方向移动,故V(正)<V(逆),故答案为:<;
(4)以反应①中生成的CaS为原料,在一定条件下经原子利用率100%的高温反应,可再生CaSO4,则另一种反应为为氧气,该反应的化学方程式为 CaS+2O2$\frac{\underline{\;高温\;}}{\;}$CaSO4;在一定条件下,CO2可与对二甲苯反应,对二甲苯的结构简式为: ,在其苯环上引入一个羧基,相当于用羧基取代苯环上的氢原子,对二甲苯中苯环上4个H原子位置等价,则该产物的结构简式为:
,在其苯环上引入一个羧基,相当于用羧基取代苯环上的氢原子,对二甲苯中苯环上4个H原子位置等价,则该产物的结构简式为: ,
,
故答案为:CaS+2O2$\frac{\underline{\;高温\;}}{\;}$CaSO4; ;
; .
.
点评 本题主要考查了影响平衡移动的因素、盖斯定律应用、平衡常数的计算等,题目难度中等,侧重于考查学生对基础知识的综合应用能力和计算能力.

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案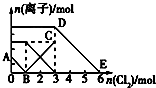 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )| A. | 线段BC代表Fe3+物质的量的变化情况 | |
| B. | 原混合溶液中n(FeBr2)=3mol | |
| C. | 当通入2molCl2时,溶液中已发生的离子反应为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | |
| D. | 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
 +3Fe+6HCl→
+3Fe+6HCl→ +3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )
+3FeCl2+2H2O,产物苯胺还原性强,易被氧化,则由甲苯合成对氨基苯甲酸的步骤合理的是( )| A. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| B. | 甲苯$\stackrel{氧化甲基}{→}$X$\stackrel{硝化}{→}$Y$\stackrel{还原硝基}{→}$对氨基苯甲酸 | |
| C. | 甲苯$\stackrel{还原}{→}$X$\stackrel{氧化甲基}{→}$Y$\stackrel{硝化}{→}$对氨基苯甲酸 | |
| D. | 甲苯$\stackrel{硝化}{→}$X$\stackrel{还原硝基}{→}$Y$\stackrel{氧化甲基}{→}$对氨基苯甲酸 |
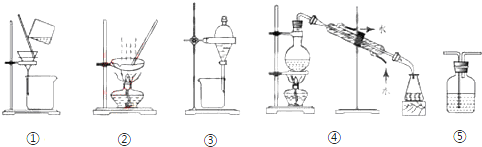
| A. | 分离Na2CO3溶液和CH3COOC2H5,选③ | B. | 用CCl4提取碘水中的碘,选② | ||
| C. | 实验室中蒸馏水的制取,选④ | D. | 粗盐提纯,选②和③ |
| A. | 测定溶液pH时,pH试纸先用蒸馏水润湿 | |
| B. | 蒸馏实验中,蒸馏前必须在蒸馏烧瓶中加入碎瓷片 | |
| C. | 用盐酸滴定滴定氨水实验中,用甲基橙作指示剂以减小实验误差 | |
| D. |  用如图所示的方法排除碱式滴定管胶管中的气泡 用如图所示的方法排除碱式滴定管胶管中的气泡 |
| A. | 反应中有水参加反应 | |
| B. | 反应后溶液呈无色 | |
| C. | 该反应的还原剂为K2S2O8 | |
| D. | MnSO4和K2S2O8的化学计量数分别为、2 |
 →合成→水热处理→过滤→水洗→表面处理→过滤水洗→干燥
→合成→水热处理→过滤→水洗→表面处理→过滤水洗→干燥 甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后,将Co2+氧化成Co3+,然后以Co3+作氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程:
甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是通电后,将Co2+氧化成Co3+,然后以Co3+作氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程: