题目内容
试管是最常用的化学仪器之一,下列清洗试管内壁吸附物质所用试剂错误的是…
- A.清洗试管内壁的MnO2--双氧水
- B.清洗试管内壁的Ag--稀硝酸
- C.清洗试管内壁的Fe2O3--稀盐酸
- D.清洗试管内壁的S--热碱液
A
分析:A.根据MnO2与浓盐酸反应生成氯化锰、氯气和水;
B.根据Ag与稀硝酸反应生成硝酸银、一氧化氮和水;
C.根据Fe2O3与稀盐酸反应生成氯化铁和水;
D.根据硫在加热条件下能与热NaOH溶液反应生成硫化钠、亚硫酸钠和水.
解答:A.MnO2与浓盐酸反应生成氯化锰、氯气和水,所以用浓盐酸清洗试管内壁的MnO2,故A错误;
B.Ag与稀硝酸反应生成硝酸银、一氧化氮和水,可用稀硝酸清洗试管内壁的Ag,故B正确;
C.Fe2O3与稀盐酸反应生成氯化铁和水,可用稀盐酸清洗试管内壁的Fe2O3,故C正确;
D.硫在加热条件下能与热NaOH溶液反应生成硫化钠、亚硫酸钠和水,可用热碱液清洗试管内壁的S,故D正确;
故选A.
点评:本题考查洗涤玻璃仪器,掌握物质的性质是解题的关键.
分析:A.根据MnO2与浓盐酸反应生成氯化锰、氯气和水;
B.根据Ag与稀硝酸反应生成硝酸银、一氧化氮和水;
C.根据Fe2O3与稀盐酸反应生成氯化铁和水;
D.根据硫在加热条件下能与热NaOH溶液反应生成硫化钠、亚硫酸钠和水.
解答:A.MnO2与浓盐酸反应生成氯化锰、氯气和水,所以用浓盐酸清洗试管内壁的MnO2,故A错误;
B.Ag与稀硝酸反应生成硝酸银、一氧化氮和水,可用稀硝酸清洗试管内壁的Ag,故B正确;
C.Fe2O3与稀盐酸反应生成氯化铁和水,可用稀盐酸清洗试管内壁的Fe2O3,故C正确;
D.硫在加热条件下能与热NaOH溶液反应生成硫化钠、亚硫酸钠和水,可用热碱液清洗试管内壁的S,故D正确;
故选A.
点评:本题考查洗涤玻璃仪器,掌握物质的性质是解题的关键.

练习册系列答案
相关题目
瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色有刺激性气味的气体──氯气.某实验小组的同学运用这一原理设计如图所示的实验装置制取干燥的氯气,并通过实验研究氯气的性质.
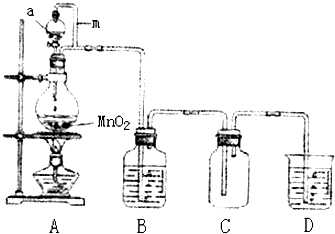
(1)仪器a的名称是______,B中盛放的试剂是______,D中盛放的试剂是______.
(2)向集满氯气的矿泉水瓶C中加入少量水,振荡后瓶子变瘪,溶液变成浅黄色,由此可得出的结论是:______.
(3)取少量(2)中所得溶液滴入到紫色石蕊溶液中,溶液先变为红色后又褪色.甲同学认为氯气与水发生了化学反应,生成物中有盐酸,验证有Cl-所需要的试剂是______.
乙同学认为氯气与水发生化学反应还有一种产物Q、盐酸、Cl2和Q三种物质均可使石蕊溶液褪色,他选用下列实验用品进行实验探究,请将实验报告填写完整.
实验用品:①石蕊溶液;②蓝石蕊试纸;③盛有盐酸的试管;④盛有氯水的试管;⑤充有干燥氯气的试管.
| 用品(填序号) | 现象 | 结论 | |
| 实验1 | ①③ | 溶液呈红色 | ______ |
| 实验2 | ______ | ______ | Cl2没有漂白性 |
| 实验3 | ______ | ______ | Q具有漂白性 |
现有下列十种物质:①Cu(OH)2 ②干冰 ③Cu ④纯碱 ⑤BaCl2 ⑥Ca(OH)2 ⑦稀硝酸 ⑧盐酸 ⑨A12(SO4)3 ⑩KHSO4
(1)按物质的分类方法填写表格的空白处(填写序号):
| 分类标准 | 氧化物 | 非电解质 |
| 属于该类的物质 |
写出④在水中的电离方程式为______.
(2)写出下列物质相互之间反应的离子方程式:⑤+⑨______
②(过量)通入浑浊的⑥溶液后变澄清______
(3)经测定0.1mol/L⑩的水溶液与0.1mol/L⑧中的氢离子浓度基本相同,往固体①中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是______.
(4)③与⑦发生反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有19.2gCu发生反应时,转移电子的物质的量为______mol,产生的NO在标准状况下的体积为______L.
 Ⅰ和
Ⅰ和 Cs,前者比后者少3个中子
Cs,前者比后者少3个中子