题目内容
设NA 为阿伏伽德罗常数的数值,下列说法正确的是
- A.1mol NaCl中,Na+的核外电子总数为10NA
- B.1mol Fe与过量的稀HNO3反应,转移2NA个电子
- C.0.1mol·L?1 Na2SO4液含有0.1NA个SO42-
- D.常温常压下,22.4L氯气与足量镁粉充分反应,生成MgBr2 2NA
A
试题分析:选项A、钠离子的核外电子数为10,因此1mol NaCl中,Na+的核外电子总数为10NA。
选项B、稀硝酸具有氧化性,能将铁氧化成铁离子。因此此过程中转移的电子数应为3NA。
选项C、因没有给出具体体积,因此无法得出溶液中溶质的物质的量,因此无法计算出溶液中离子的个数。
选项D、常温常压下,不能用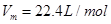 进行计算,因此错误。综上,答案为A。
进行计算,因此错误。综上,答案为A。
考点:阿伏伽德罗常数
点评:对阿伏伽德罗常数的考查,是历年高考的重点内容。考题中多结合物质的量、气体摩尔体积、电子的转移等内容。在学习中,应注意将相关联到的知识整理形成系统。
试题分析:选项A、钠离子的核外电子数为10,因此1mol NaCl中,Na+的核外电子总数为10NA。
选项B、稀硝酸具有氧化性,能将铁氧化成铁离子。因此此过程中转移的电子数应为3NA。
选项C、因没有给出具体体积,因此无法得出溶液中溶质的物质的量,因此无法计算出溶液中离子的个数。
选项D、常温常压下,不能用
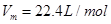 进行计算,因此错误。综上,答案为A。
进行计算,因此错误。综上,答案为A。考点:阿伏伽德罗常数
点评:对阿伏伽德罗常数的考查,是历年高考的重点内容。考题中多结合物质的量、气体摩尔体积、电子的转移等内容。在学习中,应注意将相关联到的知识整理形成系统。

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的值,下列叙述中正确的是( )
| A、常温常压下,3.2g O3所含电子数为1.2NA | B、标准状况下,2.24L CCl4中含有的C-Cl键的数目为0.4NA | C、标准状况下,11.2L NO与11.2L O2混合后所含原子数为2NA | D、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA Fe3+ |