题目内容
工业制备氯化铜时,将浓盐酸用蒸汽加热至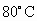 左右,慢慢加入粗CuO粉末(含杂质
左右,慢慢加入粗CuO粉末(含杂质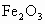 、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的
、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的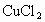 溶液,采用以下步骤[参考数据:
溶液,采用以下步骤[参考数据: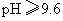 时,
时,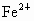 完全水解成
完全水解成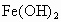 ;
;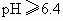 时,
时,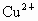 完全水解成
完全水解成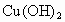 ;
;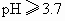 时,
时,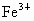 完全水解成
完全水解成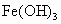 ].请回答以下问题:
].请回答以下问题:
(1)第一步除去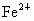 ,能否直接调整pH=9.6将
,能否直接调整pH=9.6将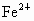 沉淀除去?________,理由是_____________________.有人用强氧化剂NaClO将
沉淀除去?________,理由是_____________________.有人用强氧化剂NaClO将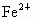 氧化为
氧化为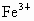 :
:
①加入NaClO后,溶液的pH变化是________.
A.一定增大
B.一定减小
C.可能增大
D.可能减小
②你认为用NaClO作氧化剂是否妥当?______________,理由是__________________.
现有下列几种常用的氧化剂,可用于除去混合溶液中的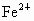 的有________(有几个选几个).
的有________(有几个选几个).
A.浓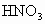
B.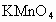
C.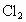
D.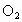
E.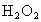
(2)除去溶液中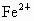 的方法是调整溶液的pH=9.6,现有下列试剂均可以使强酸性溶液的pH调整到9.6,可选用的有________(多选不限).
的方法是调整溶液的pH=9.6,现有下列试剂均可以使强酸性溶液的pH调整到9.6,可选用的有________(多选不限).
A.NaOH
B.氨水
C.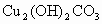
D.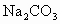
E.CuO
F.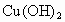
答案:略
解析:
解析:
|
答案: (1)不能;因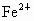 沉淀的pH最大, 沉淀的pH最大,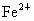 沉淀完全时 沉淀完全时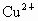 、 、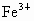 亦沉淀 ①A ②不妥当;引入新杂质 亦沉淀 ①A ②不妥当;引入新杂质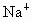 ;C、D、E (2)C、E、F ;C、D、E (2)C、E、F
解析:此题综合性强,考查思维的严密性和前后知识的联系.由题意可知: 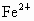 沉淀的 沉淀的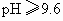 ,如果直接调整 ,如果直接调整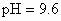 , ,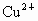 、 、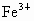 先于 先于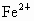 沉淀(这两种离子沉淀的pH均比 沉淀(这两种离子沉淀的pH均比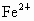 沉淀的pH小),故不能直接调整 沉淀的pH小),故不能直接调整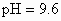 ,可将 ,可将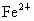 氧化成 氧化成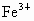 .NaClO在酸性条件下与 .NaClO在酸性条件下与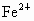 的反应是: 的反应是: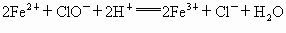 由于反应过程中要消耗 由于反应过程中要消耗 ,溶液pH一定升高.NaClO可以将 ,溶液pH一定升高.NaClO可以将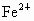 氧化成 氧化成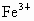 ,但引入了新杂质 ,但引入了新杂质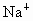 ,实际上不能采用.必须应用既能氧化 ,实际上不能采用.必须应用既能氧化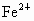 又不能引入新杂质的氧化剂,例如 又不能引入新杂质的氧化剂,例如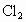 、 、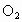 、 、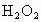 .同理,调整pH所选用的试剂可以是CuO、 .同理,调整pH所选用的试剂可以是CuO、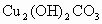 、 、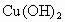 等不会引入新杂质的物质. 等不会引入新杂质的物质.
点评:盐类水解的知识在日常生活和工农业生产中都有广泛的应用,要注意理论和实际的结合,使盐类水解有更广泛的应用. |

练习册系列答案
相关题目