题目内容
取质量相等的两份铝屑,一份与100mL 1mol?L-1 HCl反应,另一份与100mL 1mol?L-1 NaOH溶液充分反应,产生的H2体积比为1:2(相同条件),则每份铝屑的质量为( )
| A、0.9g |
| B、2.7g |
| C、1.8 g |
| D、无法计算 |
考点:铝的化学性质,化学方程式的有关计算
专题:计算题
分析:根据铝跟盐酸或氢氧化钠溶液都能发生反应,利用化学方程式的特点即可看出生成相同质量的氢气时金属质量的多少.
解答:
解:观察铝反应得到氢气的方程式:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,发现了如下的规律.当都生成相同的氢气时消耗的铝的质量应该相等,也就是质量比是1:1,取质量相等的两份铝屑,一份与100mL 1mol?L-1 HCl反应,另一份与100mL 1mol?L-1 NaOH溶液充分反应,产生的H2体积比为1:2,说明与盐酸反应的时铝过量,氢氧化钠溶液过量,依据2Al+6HCl=2AlCl3+3H2↑,计算反应铝的质量=
mol×27g/mol×2=1.8g;
故选C.
| 0.1 |
| 3 |
故选C.
点评:本题主要考查学生对参加反应的物质质量数的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将右图所示实验装置,下列判断正确的是( )
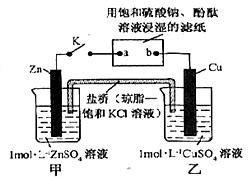

| A、电子沿Zn→a→b→Cu路径流动 |
| B、铜电极上发生氧化反应 |
| C、盐桥中的K+向甲烧杯移动 |
| D、片刻后可观察到滤纸a点变红色 |
一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+2B(g)?2C(g).该反应进行到一定限度后达到了化学平衡,不能做为判断该化学平衡标志的是( )
| A、容器内气体A的物质的量不再随时间而改变 |
| B、容器内气体C的浓度不再随时间而改变 |
| C、单位时间内生成amol物质A,同时生成3amol物质B |
| D、单位时间内生成amol物质A,同时生成2amol物质C |
下列说法正确的是( )
| A、在炽热碎瓷片的作用下,石蜡油分解产生了可以使酸性高锰酸钾溶液褪色的乙烯 |
| B、葡萄糖遇碘水会变蓝,油脂是产生能量最高的营养物质 |
| C、煤经过气化和液化等物理变化可以转化为清洁燃料 |
| D、甲苯能与溴水反生化学反应,乙醇不能发生加成反应 |
将过氧化钠固体粉末包在棉花团中,用导管往其中吹气,一会儿,棉花突然燃烧起来.下面有关该过程的说法错误的是( )
| A、该过程为放热过程 |
| B、该过程主要是口中吹过去的氧气把棉花氧化了 |
| C、该过程中CO2与过氧化钠发生了反应 |
| D、如果在包有过氧化钠粉末的棉花团中滴加少量水也可能燃烧起来 |
下列反应属于非氧化还原反应的是( )
A、Fe2O3+3CO
| ||||
B、NH4NO3
| ||||
C、CaCO3
| ||||
D、4CuO
|
在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )
| A、MnO4-、K+、Na+、SO42- |
| B、Na+、K+、HCO3-、Cl- |
| C、Mg2+、NH4+、Cl-、NO3- |
| D、Ba2+、K+、S2-、SO42- |