题目内容
【题目】(1)在 20mL 0.0020mol·L-1NaCl 溶液中加入 20 mL 0.020mol·L-1 AgNO3 溶液,________(有、无)AgCl 沉淀生成 ,此时溶液中 Cl-离子浓度为 _____mol·L-1。已知 AgCl 的 Ksp=1.8×10-10
(2)下列物质中属于强电解质且能导电的是________
①固体食盐 ②熔融 KNO3 ③CuSO4·5H2O ④液溴 ⑤蔗糖 ⑥CO2 气体 ⑦盐酸 ⑧液态醋
(3)1gH2 完全燃烧生成液态水时放出 142.5kJ 的热量,写出表示 H2 燃烧热的热化学方程式________。
【答案】有 2×10-8 ② H2(g)+ ![]() O2(g)=H2O(l) H=-285 kJ/mol。
O2(g)=H2O(l) H=-285 kJ/mol。
【解析】
(1)等体积混合浓度减半,c(Cl-)=0.0010mol/L,c(Ag+)=0.010mol/L,AgNO3过量,Qc=0.0010 mol/L×0.010 mol/L=1×10-5> Ksp=1.8×10-10,有AgCl沉淀生成;溶液中剩余的银离子的量为:n(Ag+)=n(Ag+)-n(Cl-)=0.02L×0.020mol·L-1-0.02L ×0.0020mol·L-1=3.6×10-4mol,c(Ag+)=![]() =9×10-3mol/L,根据AgCl的 Ksp=1.8×10-10可知,此时溶液中c(Cl-)=
=9×10-3mol/L,根据AgCl的 Ksp=1.8×10-10可知,此时溶液中c(Cl-)= ![]() =2×10-8mol/L;
=2×10-8mol/L;
故答案为:有;2×10-8;
(2)①固体食盐不是纯净物,不属于电解质,也不能导电;②熔融KNO3 能导电,且是强电解质;③CuSO4·5H2O是电解质,但不能导电;④液溴为单质,不是电解质,也不能导电;⑤蔗糖属于非电解质,不能导电;⑥CO2气体属于非电解质,不能导电;⑦盐酸为混合物,不属于电解质,但能导电;⑧液态醋是弱电解质,不能导电;故选②;
故答案为:②;
(3)燃烧热是指1mol纯物质与氧气反应完全燃烧生成稳定的氧化物所放出的能量,1gH2为0.5mol,完全燃烧生成液态水时放出142.5KJ 的热量,燃烧热的热化学反应方程式为:H2(g)+ ![]() O2(g)=H2O(l) H=-285kJ/mol;
O2(g)=H2O(l) H=-285kJ/mol;
故答案为:H2(g)+ ![]() O2(g)=H2O(l) H=-285 kJ/mol。
O2(g)=H2O(l) H=-285 kJ/mol。

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案【题目】含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有 K2Cr2O7 的废水并回收重铬酸,具体的流程如下:
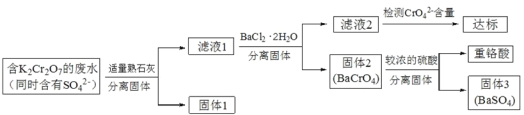
已知:CaCr2O7、BaCr2 O7 易溶于水,其它几种盐在常温下的溶度积如下表所示。
物质 | CaSO4 | CaCrO4 | BaCrO4 | BaSO4 |
溶度积 | 9.1106 | 2.30 102 | 1.17 1010 | 1.08 1010 |
(1)用离子方程式表示K2Cr2O7溶液中同时存在 K2CrO4的原因(将离子方程式补充完整):______Cr2O72-+______![]() ____CrO42+______
____CrO42+______
(2)向滤液 1 中加入 BaCl2 ![]() 2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
2H2O 的目的是使 CrO42- 从溶液中沉淀出来。
①结合上述流程说明熟石灰的作用:_____。
②结合表中数据,说明选用Ba2 不选用Ca2处理废水的理由:_____。
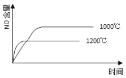
③ 研究温度对CrO42 沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下CrO42- 的沉淀率(沉淀率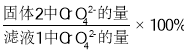 如图所示)
如图所示)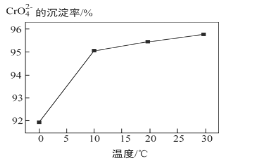
已知:![]()
CrO42- 的沉淀效率随温度变化的原因是_____。
(3)向固体2中加入硫酸,回收重铬酸。
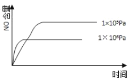
①硫酸浓度对重铬酸的回收率如下图(左)所示。结合化学平衡移动原理,解释使用 0.450 mol/L 的硫酸时,重铬酸的回收率明显高于使用 0.225 mol/L 的硫酸的原因:_____。
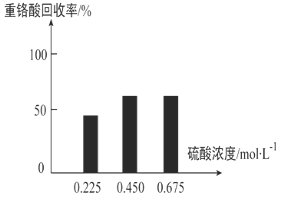
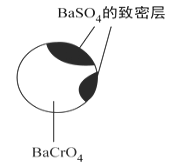
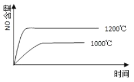
②回收重铬酸的原理如上图(右)所示。当硫酸浓度高于0.450 mol/L时,重铬酸的回收率没有明显变化,其原因是_____。
(4)综上所述,沉淀BaCrO4进一步回收重铬酸的效果与_____、_____、有关。