题目内容
常温常压下,1g H2在足量Cl2中燃烧生成HCl气体,放出 92.3kJ的热量,则该反应的热化学方程式书写正确的是( )
| A、H2(g)+Cl2(g)?2HCl(g);△H=-92.3 kJ/mol | B、H2(g)+Cl2(g)?HCl(g);△H=+92.3kJ/mol | C、H2+Cl2?2HCl;△H=-184.6kJ/mol | D、2HCl(g)?H2(g)+Cl2(g);△H=+184.6kJ/mol |
分析:A、2g氢气完全燃烧放热184.6KJ;
B、反应是放热反应,焓变为负值;
C、热化学方程式需要标注物质聚集状态;
D、反应逆向进行焓变符合相反;
B、反应是放热反应,焓变为负值;
C、热化学方程式需要标注物质聚集状态;
D、反应逆向进行焓变符合相反;
解答:解:A、常温常压下,1g H2在足量Cl2中燃烧生成HCl气体,放出 92.3kJ的热量,2g氢气完全燃烧放热184.6KJ,H2(g)+Cl2(g)═2HCl(g);△H=-184.6 kJ/mol,故A错误;
B、反应是放热反应,焓变为负值,故B错误;
C、热化学方程式需要标注物质聚集状态,选项中 物质状态未标注,故C错误;
D、反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g);△H=-184.6 kJ/mol,反应逆向进行焓变符合相反,热化学方程式为2HCl(g)═H2(g)+Cl2(g);△H=+184.6kJ/mol;故D正确;
故选:D.
B、反应是放热反应,焓变为负值,故B错误;
C、热化学方程式需要标注物质聚集状态,选项中 物质状态未标注,故C错误;
D、反应的热化学方程式为:H2(g)+Cl2(g)═2HCl(g);△H=-184.6 kJ/mol,反应逆向进行焓变符合相反,热化学方程式为2HCl(g)═H2(g)+Cl2(g);△H=+184.6kJ/mol;故D正确;
故选:D.
点评:本题考查了热化学方程式的书写方法和注意问题,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
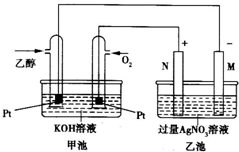 某乙醇燃料电池工作时的装置如图所示,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少.
某乙醇燃料电池工作时的装置如图所示,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少. 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.
