题目内容
3.将一小块Na投入到足量的CuSO4溶液中,现象描述正确的是( )| A. | 置换出金属铜 | B. | 产生气体,置换出金属铜 | ||
| C. | 只生成蓝色沉淀 | D. | 产生气体,生成蓝色沉淀 |
分析 钠投入硫酸铜溶液,先与水反应生成氢氧化钠和氢气,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,据此解答.
解答 解:钠投入硫酸铜溶液,先与水反应生成氢氧化钠和氢气,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,方程式为:2Na+2H2O=2NaOH+H2↑、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,既有气体产生又有沉淀生成,
故选D.
点评 本题考查了钠与硫酸铜溶液的反应,明确钠的化学性质是解题关键,注意钠与盐溶液反应的过程,题目难度不大.

练习册系列答案
相关题目
14.下列对实验操作分析错误的是( )
| A. | 配制0.1mol/L NaCl溶液时,若没有洗涤烧杯和玻璃棒,则所得溶液物质的量浓度偏低 | |
| B. | NH4NO3溶解吸热,若配制0.5mol/L H4NO3溶液时直接将溶解后的溶液转移到容量瓶中,则所得溶液的物质的量浓度偏高 | |
| C. | 配制一定物质的量浓度溶液时,若所用砝码已经生锈,则所得溶液的物质的量浓度偏高 | |
| D. | 配制一定物质的量浓度溶液时,若定容中不小心加水超过刻度线,立刻将超出的水吸出,则所得溶液的物质的量浓度偏低 |
11.镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中的总反应方程式是:Ni(OH)2+M=NiOOH+MH,已知:6NiOOH+NH3+H2O+OH-=6Ni(OH)2+NO2- 下列说法正确的是( )
| A. | 充电过程中OH-离子从阳极向阴极迁移 | |
| B. | 充电过程中阴极的电极反应式:H2O+M+e-=MH+OH-,H2O中的H被M还原 | |
| C. | 电池放电过程中,正极电极反应式为:NiOOH+H2O+e-=Ni(OH)2+OH- | |
| D. | NiMH电池中可以用KOH溶液、氨水等作为电解质溶液 |
7. 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间的变化如图所示.下列说法正确的是( )
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间的变化如图所示.下列说法正确的是( )
 一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间的变化如图所示.下列说法正确的是( )
一定温度下,将1mol A和1mol B气体充入2L恒容密闭容器中,发生反应A(g)+B(g)?xC(g)+D(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间的变化如图所示.下列说法正确的是( )| A. | 反应方程式中的x=1 | |
| B. | t2时刻改变的条件是使用催化剂 | |
| C. | t3时刻改变的条件是移去少量物质D | |
| D. | t1~t3间该反应的平衡常数均为4 |
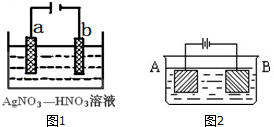 金属冶炼和处理常涉及电化学反应.
金属冶炼和处理常涉及电化学反应.