��Ŀ����
��֪���ȼ��a g��Ȳ����ʱ����1 mol������̼�����Һ̬ˮ�����ų�����b kJ������Ȳȼ�յ��Ȼ�ѧ����ʽ��ȷ���� �� ��
A��2C2H2��g��+5O2��g�� 4CO2��g��+2H2O��l������H=��4b
kJ/mol
B��C2H2��g��+ O2��g��
O2��g��
2CO2��g��+H2O��l������H=2b
kJ/mol
C��2C2H2��g��+5O2��g�� 4CO2��g��+2H2O��l������H=��2b
kJ/mol
D��2C2H2��g��+5O2��g�� 4CO2��g��+2H2O��l������H=b kJ/mol
�������������Ȼ�ѧ����ʽ����д����Ȳȼ���Ƿ��ȷ�Ӧ����H��0��B��D����ȷ�����������֪ÿ����1molCO2�ͷų�bkJ������������ȷ�Ĵ���A��
���𰸡�
A

��ϰ��ϵ�д�
 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
�����Ŀ

 ��B2H6Ϊ�����飩
��B2H6Ϊ�����飩

 ��B2H6Ϊ�����飩
��B2H6Ϊ�����飩
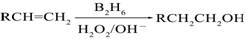 ��B2H6Ϊ�����飩
��B2H6Ϊ�����飩