题目内容
化学反应N2+3H2=2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是( )

A.N2(g)+3H2(g)=2NH3(1); △H=2(a-b-c)kJ·mol-1
B.N2(g)+3H2(g)=2NH3(g);△H=2(b-a)kJ·mol-1
C. N2(g)+
N2(g)+ H2(g)=NH3(1);△H=(b+c-a)kJ·mol-1
H2(g)=NH3(1);△H=(b+c-a)kJ·mol-1
D. N2(g)+
N2(g)+ H2(g)=NH3(g);
△H=(a+b)kJ·mol
H2(g)=NH3(g);
△H=(a+b)kJ·mol
【答案】
A
【解析】
试题分析:根据图像可知,反应物的总能量高于生成物的总能量,所以是正反应是放热反应,A正确,C不正确;如果生成物是氨气,则反应的热化学方程式是N2(g)+3H2(g)=2NH3(g);△H=-2(b-a)kJ·mol-1,因此B和D都是错误的,答案选A。
考点:考查反应热的判断、计算及图像识别
点评:该题是高考中的常见图像,试题结合图像分析,增加了试题的难度。该题有利于培养学生的图像识别能力和灵活应变能力,有利于培养学生应试能力,提高学生的学习效率。

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
 化学反应N2+3H2→2NH3的能量变化如图所示,该反应的热化学方程式是( )
化学反应N2+3H2→2NH3的能量变化如图所示,该反应的热化学方程式是( )| A、N2(g)+H2(g)→NH3(1)-46 kJ | B、N2(g)+H2(g)→NH3(g)-454 kJ | C、N2(g)+3 H2(g)→2 NH3(g)+92 kJ | D、N2(g)+3 H2(g)→2 NH3(1)+431.3 kJ |
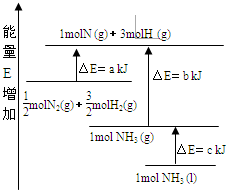 化学反应N2+3H2?2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是( )
化学反应N2+3H2?2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是( )| A、N2(g)+3H2(g)?2NH3(l);△H=2(a-b-c)kJ?mol-1 | ||||
| B、N2(g)+3H2(g)?2NH3(g);△H=2(b-a)kJ?mol-1 | ||||
C、
| ||||
D、
|
 (2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )
(2008?重庆)化学反应N2+3H2=2NH3的能量变化如图所示,该反应的热化学方程式是( )