题目内容
某恒温密闭容器中,可逆反应A(s)
 B+C(g)
ΔH=Q kJ·mol-1(Q>0 ),达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是
B+C(g)
ΔH=Q kJ·mol-1(Q>0 ),达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是
A.产物B的状态可能为固态或液态
B.平衡时,单位时间内A和B消耗的物质的量之比为1:1
C.保持体积不变,向平衡体系中加入A(s),平衡不移动
D.若开始时向容器中加入1molB和1molC,达到平衡时放出热量Q kJ
【答案】
D
【解析】
试题分析:若B是气体,平衡常数K=c(B)·c(C),若B是非气体,平衡常数K=c(C),由于C(g)的浓度不变,因此B是非气体,A正确;C项:A为固体,加入A(s),平衡不移动;根据平衡的v(正)=v(逆)可知B正确;由于反应是可逆反应,因此达到平衡时放出热量小于Q,D项错误。
考点:本题考查化学平衡、可逆反应的含义。

练习册系列答案
相关题目
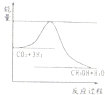
 新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由该铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中酸性氧化物分解除去,转化流程如图所示:
新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由该铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中酸性氧化物分解除去,转化流程如图所示:
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3


 若2molZnFe2Ox与足量SO2可生成1.0molS,
若2molZnFe2Ox与足量SO2可生成1.0molS,
 CH3OH(g)+H2O(g)
△H3
CH3OH(g)+H2O(g)
△H3