题目内容
能正确表示下列化学反应的离子方程式的是( )
分析:A、铁和盐酸反应生成氯化亚铁和氢气;
B、选项中电荷不守恒;
C、氯化铁和铁反应生成氯化亚铁;
D、一水合氨是弱碱存在电离平衡.
B、选项中电荷不守恒;
C、氯化铁和铁反应生成氯化亚铁;
D、一水合氨是弱碱存在电离平衡.
解答:解:A、铁与稀盐酸反应,生成氯化亚铁和氢气:Fe+2H+═Fe2++H2↑,故A错误;
B、铝粉投入到NaOH溶液中反应的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、氯化铁溶液中加入铁粉反应的离子方程式:2Fe3++Fe═3Fe2+,故C正确;
D、AlCl3溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故D错误;
故选C.
B、铝粉投入到NaOH溶液中反应的离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C、氯化铁溶液中加入铁粉反应的离子方程式:2Fe3++Fe═3Fe2+,故C正确;
D、AlCl3溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故D错误;
故选C.
点评:本题考查了离子方程式书写方法和注意问题,主要是反应实质,电荷守恒,弱电解质判断的应用,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在下列各说法中,正确的是( )
| A、对于2SO2(g)+O2(g)?2SO3(g)△H=-QkJ?mol-1,(Q>0),若反应中充入1molSO2和足量的氧气反应时,放出的热量一定是Q/2 kJ | B、热化学方程式中的化学计量数不能用分数表示 | C、Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0,该反应的化学能可以转化为电能 | D、△H的大小与热化学方程式的化学计量数无关 |
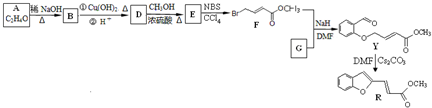
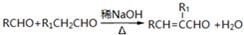 (R、R1表示烃基或氢)
(R、R1表示烃基或氢)
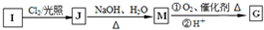


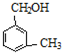 互为同系物
互为同系物