题目内容
【物质结构与性质】
(1)已知某短周期元素的电负性是同族元素中最大的,其第一电离能高于其在周期表中直接相邻的元素,其原子最外电子层电子分布在两种形状的原子轨道中。请画出该元素最外电子层的电子排布图:
(2)已知能够自由移动的(CH3)3NH+和AlCl4 -可形成离子液体,由这两种离子形成的晶体的熔点低于100℃,则由这两种离子形成的晶体属于 晶体。
(3)X+中所有电子正好全部充满K、L、M三个电子层,它与N3—形成的晶体结构,如右图所示。请回答:
①用元素符号表示X+:
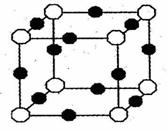 ②图中O表示的是:
②图中O表示的是:
③N3— 的配位数是
![]()
(1) (2分)
(2)离子(2分)
(3)①Cu+ (2分) ②N3-(1分) ③6(1分)

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目


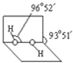 (4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取
(4)已知过氧化氢分子的空间结构如图所示,分子中氧原子采取