题目内容
2.乙烯的结构简式CH2=CH2 电子式: ;羟基的电子式:
;羟基的电子式: ;氢氧根离子的电子式
;氢氧根离子的电子式 .
.
分析 乙烯含有碳碳双键;
乙烯分子中碳碳以双键相连,碳剩余价键被H饱和,由此写出电子式;
羟基由一个氧原子和一个氢原子构成,氧原子最外层6个电子,氢原子最外层一个电子,二者形成一个共用电子对;
氢氧根离子为阴离子,电子式中需要标出原子的最外层电子及带有的电荷.
解答 解:乙烯含有碳碳双键,结构简式为CH2=CH2;
乙烯分子中碳碳以双键相连,碳剩余价键被H饱和,由此写出电子式为 ;
;
羟基中存在一个氧、氢共用电子对,羟基的电子式为: ;
;
氢氧根离子为阴离子,电子式中需要标出电荷及原子的最外层电子,氢氧根离子的电子式为: ,
,
故答案为:CH2=CH2; ;
; ;
; .
.
点评 本题考查了常见化学用语的表示方法,题目难度中等,注意掌握电子式、结构简式等化学用语的概念及正确的表示方法.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 铜和盐酸不是化台物,能导电是电解质 | |
| B. | 可用过的量氢氧化钠区别镁离子和铝离子 | |
| C. | 钾的焰色反应是白色的 | |
| D. | 二氧化硫有毒,不能漂白食品,亦不能用作食品防腐剂 |
10.某离子反应中共有H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中c(ClO-)随反应进行逐渐减小.下列判断错误的是( )
| A. | 该反应的还原剂是NH4+ | |
| B. | 氧化剂与还原剂的物质的量之比是2:3 | |
| C. | 消耗1mol氧化剂,转移2mol电子 | |
| D. | 反应后溶液酸性明显增强 |
17.在甲、乙两个密闭容器中.分别充有质量相同的O2、H2两种气体,若两容器温度和密度均相同,则下列说法正确的是( )
| A. | 甲的体积比乙的体积大 | B. | 甲的分子数比乙的分子致少 | ||
| C. | 甲的压强比乙的压强大 | D. | 甲的摩尔体积比乙的华尔体积大 |
7.下列叙述正确的是( )
| A. | 胶体区别于其他分散系的根本原因是胶体有丁达尔现象 | |
| B. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<浊液<胶体 | |
| C. | 有单质参加或有单质生成的反应一定是氧化还原反应 | |
| D. | 失电子的反应物在反应中作还原化剂,反应中被氧化 |
14.将3mol•L-1的Ca(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为( )
| A. | $\frac{6a}{b}$ mol•L-1 | B. | $\frac{3a}{b}$ mol•L-1 | C. | $\frac{3b}{a}$ mol•L-1 | D. | $\frac{b}{a}$ mol•L-1 |
12.下列不能使KI-淀粉溶液变蓝的是( )
| A. | SO2 | B. | H2O2 | C. | Cl2 | D. | 碘酒 |
 ,用电子式表示C、D两元素形成化学键的过程:
,用电子式表示C、D两元素形成化学键的过程: .
. .
. 反应类型加聚反应
反应类型加聚反应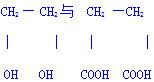 的聚合反应n HOCH2CH2OH+n HOOCCH2CH2COOH
的聚合反应n HOCH2CH2OH+n HOOCCH2CH2COOH 
 +(2n-1)H2O反应类型缩聚反应
+(2n-1)H2O反应类型缩聚反应 反应类型取代反应
反应类型取代反应