题目内容
12.MgBr2和MgO的混合物共10g,经分析,其中Mg元素的质量分数为38.4%,则Br元素的质量分数为( )| A. | 30% | B. | 40% | C. | 50% | D. | 46% |
分析 设出混合物中含有溴元素的质量,然后根据n=$\frac{m}{M}$计算出镁离子、氧离子、溴离子的物质的量,再根据正负总电荷为0列式计算出溴的质量,最后计算出溴元素的质量分数.
解答 解:设混合物中含有溴元素的质量为x,
该10g混合物中含有镁离子的物质的量为$\frac{10g×38.4%}{24g/mol}$=0.16mol,
含有氧离子的物质的量为:$\frac{10g×(1-38.4%)-x}{16g/mol}$,
含有溴离子的物质的量为:$\frac{x}{80g/mol}$,
该混合物中总电荷一定为0,则:0.16mol×2=$\frac{10g×(1-38.4%)-x}{16g/mol}$×2+$\frac{x}{80g/mol}$×1,
解得:x=4g,
所以混合物中溴元素的质量分数为$\frac{4g}{10g}$×100%=40%,
故选B.
点评 本题考查了元素质量分数的计算,题目难度不大,明确物质的量与摩尔质量的关系为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
2.下列关于物质的量的叙述正确的是( )
| A. | 表示物质微粒个数的物理量 | B. | 表示物质微粒集体的物理量 | ||
| C. | 表示物质质量的物理量 | D. | 表示物质的质量和个数的物理量 |
3.CO2的资源化利用是解决温室效应的重要途径,在一定条件下利用NH3 捕获CO2 生成重要化工产品三聚氰酸( )下列关于三聚氰酸的说法正确( )
)下列关于三聚氰酸的说法正确( )
 )下列关于三聚氰酸的说法正确( )
)下列关于三聚氰酸的说法正确( )| A. | 三聚氰酸属于单质 | B. | 三聚氰酸属于氧化物 | ||
| C. | 三聚氰酸属于有机化合物 | D. | 三聚氰酸属于混合物 |
7.对于反应A+B-→C,如果温度每升高10℃,反应速率增加为原来的3倍.在10℃时,完成反应的20%需要54min;将温度提高到40℃,完成反应的20%需要的时间为( )
| A. | 2 min | B. | 3 min | C. | 6 min | D. | 9 min |
17.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
| A. | NH4+、Cu2+、Cl-、NO3- | B. | K+、Na+、SO32-、S2- | ||
| C. | K+、Na+、CO32-、SO42- | D. | Ba2+、Na+、HCO3-、Br- |
4.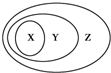 下表所列的一些物质或概念间的从属关系中,不符合图示要求的是( )
下表所列的一些物质或概念间的从属关系中,不符合图示要求的是( )
 下表所列的一些物质或概念间的从属关系中,不符合图示要求的是( )
下表所列的一些物质或概念间的从属关系中,不符合图示要求的是( )| X | Y | Z | |
| 例 | 氧化物 | 化合物 | 纯净物 |
| A | 碱 | 电解质 | 化合物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 酸性氧化物 | 非金属氧化物 | 化合物 |
| D | 碱性氧化物 | 金属氧化物 | 氧化物 |
| A. | A | B. | B | C. | C | D. | D |
2.互为同分异构体的物质一定不可能具有( )
| A. | 相同的分子式 | B. | 相同的结构 | ||
| C. | 相似的化学性质 | D. | 相同的相对分子质量 |

