题目内容
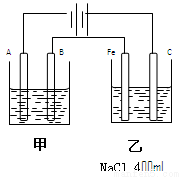
(16分)如图为相互串联的甲乙两个电解池,
请回答:
(1)甲池若为电解精炼铜的装置,A极是 ,材料是 ,电极反应为 ,B极是 ,材料是 ,电极反应为 。
(2)若甲槽阴极增重12.8g,则乙槽阴极放出气体在标准状况下的体积为 。
(3)若乙槽剩余液体为400mL,求电解后得到碱液的物质的量浓度 。
(1)阴极, 精铜,Cu2+ + 2e- = Cu; 阳极,粗铜, Cu - 2e- = Cu2+,(2)4.48L。 (3)1mol/L。
【解析】
试题分析:(1)A极与电源的负极相连,作为阴极,所以连接的是纯铜,则电极反应式为Cu2+ + 2e–= Cu;B电极就是阳极,连接的是粗铜,电极反应式是Cu -2e–= Cu2+。乙池中C电极是阳极,铁是阴极,电解饱和食盐水,则总的离子方程式是2Cl- + 2H2O  Cl2↑ + 2OH- + H2 ↑。
Cl2↑ + 2OH- + H2 ↑。
(2)甲槽阴极增重12.8g,则析出铜是12.8g,物质的量是0.2mol,转移电子是0.4mol。则根据电子的得失守恒可知,乙槽阴极放出氢气体积是0.2mol×22.4L/mol=4.48L。
(3)根据(2)可知,氢气是0.2mol,则生成氢氧化钠是0.4mol,物质的量浓度是0.4mol÷0.4L=1.0mol/L。
考点:考查电极名称判断、电极反应式的书写、电极产物的计算。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
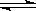 2B(g) + C(g)中,生成物C在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2B(g) + C(g)中,生成物C在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是