题目内容
现有一瓶甲、乙的混合物,已知甲、乙属同系物,甲、乙某些性质如下:
| 物质 | 分子式 | 熔点(℃) | 沸点(℃) | 密度(g/cm3) | 水溶性 |
| 甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
- A.蒸馏
- B.萃取
- C.加热升华
- D.分液
分析:互溶且沸点不同的液体采用蒸馏的方法分离.
解答:根据题中信息可以看出,甲和乙两物质的熔点相差不大,均易溶于水,能互溶,但是沸点相差较大,所以可以采用蒸馏的方法通过控制沸点的不同来实现二者的分离,故选A.
点评:本题考查物质的分离、提纯的基本方法选择与应用,难度不大,熟记常见物质的分离方法和原理是解题的关键所在.

 走进文言文系列答案
走进文言文系列答案某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,该小组同学开始了实验探究。
⑴实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体。记录单位时间氢气产生的体积。
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
其中:V1= ,V6= ,V9= ;
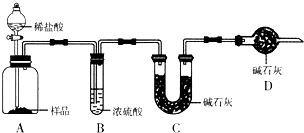
⑵实验装置:甲同学拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
 ④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
④ 乙同学认为可选用右图装置中的_____(填A或B)直接与锥形瓶的导管A相连用以测量氢气的体积,理由是 ;实验结束时量筒内的液面高于水槽中液面,立即读数会使氢气的总体积 (填“偏大”“偏小”或“不变”);应进行的操作是 ;
⑶实验现象与结论:反应一段时间后,实验A中的金属呈 色,实验E中的金属呈 色;该学习小组最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
⑷问题讨论:实验室中现有![]() 、
、![]() 、
、![]() 、
、![]() 等4种溶液,可与实验中
等4种溶液,可与实验中![]() 溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
溶液起相似作用的是 ;要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);


 现有甲、乙、丙三个学生,欲测定某工业纯碱样品中Na2CO3的质量分数(纯碱样品中Na2CO3的质量分数为92%~96%),分别设计如下实验方案,请你帮助他们完成实验.
现有甲、乙、丙三个学生,欲测定某工业纯碱样品中Na2CO3的质量分数(纯碱样品中Na2CO3的质量分数为92%~96%),分别设计如下实验方案,请你帮助他们完成实验.