题目内容
固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验。
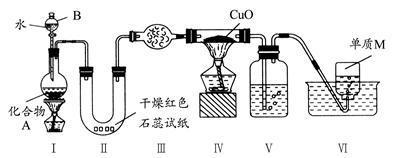
(1)仪器B的名称是________。
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为________;Ⅳ中发生反应的化学方程式为________;V中的试剂为________。
(3)乙组同学进行同样实验,但装置连接顺序为ⅠⅢⅣⅡVⅥ,此时Ⅱ中现象为________,原因是________。
(4)经上述反应,2.5 g化合物A理论上可制得0.56 L(标准状况)M,则A的化学式为________。

(1)仪器B的名称是________。
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为________;Ⅳ中发生反应的化学方程式为________;V中的试剂为________。
(3)乙组同学进行同样实验,但装置连接顺序为ⅠⅢⅣⅡVⅥ,此时Ⅱ中现象为________,原因是________。
(4)经上述反应,2.5 g化合物A理论上可制得0.56 L(标准状况)M,则A的化学式为________。
(1)分液漏斗 (2)碱石灰;3CuO+2NH3 3Cu+N2+3H2O;浓H2SO4 (3)试纸变蓝;氧化铜与氨气反应生成的水和未反应的氨气形成氨水,使红色石蕊试纸变蓝
3Cu+N2+3H2O;浓H2SO4 (3)试纸变蓝;氧化铜与氨气反应生成的水和未反应的氨气形成氨水,使红色石蕊试纸变蓝
(4)Mg3N2
 3Cu+N2+3H2O;浓H2SO4 (3)试纸变蓝;氧化铜与氨气反应生成的水和未反应的氨气形成氨水,使红色石蕊试纸变蓝
3Cu+N2+3H2O;浓H2SO4 (3)试纸变蓝;氧化铜与氨气反应生成的水和未反应的氨气形成氨水,使红色石蕊试纸变蓝(4)Mg3N2
(1)带有活塞的漏斗是分液漏斗。(2)根据实验流程图可知,用红色石蕊试纸检验的是氨气,氨气是一种碱性气体,用碱石灰干燥氨气;氨气具有还原性,可将黑色的CuO还原为红色的Cu,自身被氧化为N2;尾气中的氨气被浓硫酸吸收,最后N2用排水法收集。(3)氧化铜与氨气反应生成的水和未反应的氨气形成氨水,使红色石蕊试纸变蓝。
(4)0.56 L M即N2的物质的量为0.025 mol,则化合物A中N的质量为0.7 g,则另一种元素的质量为1.8 g,经过对A中未知元素的化合价讨论可得,只能是+2价的Mg,故该物质是Mg3N2。
(4)0.56 L M即N2的物质的量为0.025 mol,则化合物A中N的质量为0.7 g,则另一种元素的质量为1.8 g,经过对A中未知元素的化合价讨论可得,只能是+2价的Mg,故该物质是Mg3N2。

练习册系列答案
相关题目
 2CuCl2+O2测定铜的近似相对原子质量,可供选择的装置如图所示。
2CuCl2+O2测定铜的近似相对原子质量,可供选择的装置如图所示。