题目内容
利用下图所示装置,分别①将SO2气体通入下列溶液;②加热一段时间;③冷却至室温。写出实验现象及结论。
A.品红溶液;B.石蕊溶液;C.溴水。
解析:“漂白性”是针对有机色素褪色,有以下三种:
(1)吸附有机色素而褪色,如活性炭吸附红墨水。
(2)与有机色素化合而褪色,如二氧化硫与品红化合生成一种不稳定的化合物,使品红褪色。若该化合物不稳定,其褪色是可逆的,上述溶液遇热分解,使品红恢复原红色。
(3)氧化剂氧化有机色素而褪色,如次氯酸使很多有色物质褪色。一般说来,因氧化还原反应而褪色,不可逆转。次氯酸、过氧化钠、双氧水等都具备“漂白性”。
除此以外,某些化学反应也能发生颜色变化。如二氧化硫和溴水发生氧化还原反应,使溴水褪色;滴有酚酞的NaOH溶液呈红色,通过过量的SO2气体后也可由红色变为无色,这不属于SO2的“漂白性”。
答案:A.首先溶液由红色变为无色,加热后溶液呈红色,冷却至室温溶液又呈无色。
结论:SO2的漂白作用是不稳定的,具有可逆性。
B.溶液由紫色变为红色,加热一段时间溶液由红色变为紫色,冷却至室温溶液由紫色变为红色。
结论:SO2的漂白作用具有局限性和选择性,对酸碱指示剂、墨水等不能漂白。亚硫酸是易分解的酸。
C.溴水溶液变为无色(溴水褪色),加热、冷却都没变化。
结论:此反应是SO2的还原性,不是漂白性。

练习册系列答案
相关题目
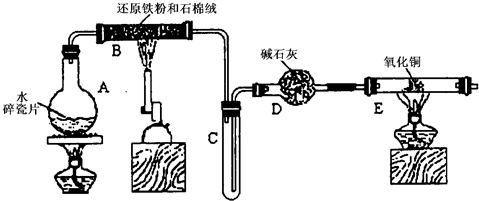
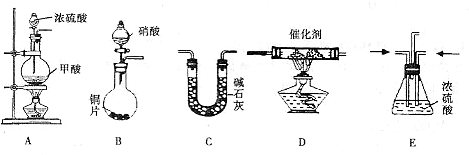
 ( )→( )→( )→收集气体
( )→( )→( )→收集气体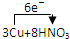 =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O (2012?济南二模)纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
(2012?济南二模)纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
 Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
Cu+Cu2++H2O,则可用来检验反应后E中的红色固体中除Cu外是否含Cu2O,可用的试剂是________(填序号)
